题目内容
7.如图为五个椭圆交叉构成的团,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、Na2CO3五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为其相应的分类标准代号.请回答下列问题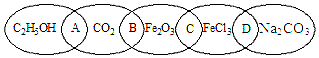
(1)分类标准代号A表示ac(可多项)
a.两物质都是非电解质 b.两物质都是有机物
c.两物质部是含碳化合物 d.两物质都是氧化物
(2)上述五种物质中的某一物质的饱和溶液中通入足量CO2,溶液中会有晶体析出.该反应的离子方程式为:2Na++CO32-+CO2+H2O=2NaHCO3↓.
分析 (1)电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等;
含碳元素的化合物为含碳化合物;
有机物即有机化合物.含碳化合物(一氧化碳、二氧化碳、碳酸、碳酸盐、金属碳化物、氰化物除外)或碳氢化合物及其衍生物的总称;
氧化物指氧元素与另外一种化学元素组成的二元化合物;
(2)上述五种物质中能和二氧化碳反应的是碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,碳酸氢钠溶解度小于碳酸钠.
解答 解:(1)a.乙醇和二氧化碳都属于非电解质,故a正确;
b.乙醇为有机物,而二氧化碳不属于有机物,故b错误;
c.乙醇和二氧化碳都是含碳化合物,故c正确;
d.二氧化碳为氧化物,而乙醇分子中含有H元素,不属于氧化物,故d错误;
故选ac;
(2)上述五种物质中能和二氧化碳反应的是碳酸钠,向饱和的碳酸钠溶液中通入二氧化碳,能生成溶解度更小的碳酸氢钠,故有晶体析出,离子方程式为:2Na++CO32-+CO2+H2O=2NaHCO3↓.
故答案为:2Na++CO32-+CO2+H2O=2NaHCO3↓.
点评 本题考查电解质和非电解质、氧化物概念的辨析、四种基本反应类型的判断、离子方程式的书写,明确相关概念是解题关键,注意碳酸钠与碳酸氢钠溶解度,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
17.分子式为C6H10O4,且能与NaHCO3反应的只含一种官能团的有机物共有(不含立体异构)( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
2.有Al、CuO、Fe2O3组成的混合物共10.0g,放入500mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250mL 2.0mol/L的NaOH溶液时,得到的沉淀最多.上述盐酸溶液的浓度为( )
| A. | 1mol/L | B. | 2 mol/L | C. | 0.5 mol/L | D. | 1.5 mol/L |
15.pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是( ),添加( )可使该溶液复原.
| A. | NaOH H2O | B. | NaCl H2O | C. | AgNO3 Ag2O | D. | Na2SO4 H2O |

 .
. .
. .
.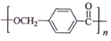 的路线:
的路线: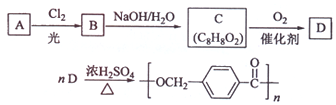
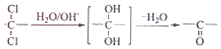
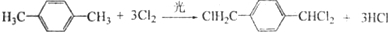 ;
;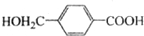 ,由D合成聚酯类高分子材料
,由D合成聚酯类高分子材料 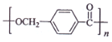 的化学方程式是n
的化学方程式是n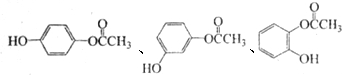 (写结构简式).
(写结构简式).