题目内容
19.已知如表数据:| 化学式 | 电离平衡常数(25℃) |
| HCN | K=5.0×10-10 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
分析 电离平衡常数越大,酸的酸性越强,根据表中数据可知酸性:H2CO3>HCN>HCO3-,向NaCN溶液中通入少量CO2,反应生成HCN和碳酸氢钠,据此写出反应的化学方程式.
解答 解:根据电离平衡常数大小可知酸性:H2CO3>HCN>HCO3-,向NaCN溶液中通入少量CO2,反应生成HCN和碳酸氢钠,不能生成二氧化碳,反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3,
故答案为:NaCN+H2O+CO2=HCN+NaHCO3.
点评 本题考查了化学方程式的书写及应用,题目难度中等,根据电离平衡常数正确判断酸性强弱为解答关键,注意掌握化学方程式的书写原则是,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
9.容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容量、④压强、⑤刻度线这五项中的( )
| A. | ②④ | B. | ③⑤ | C. | ①②④ | D. | ①③⑤ |
10.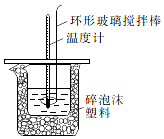 某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)环形玻璃搅拌棒的作用是使酸和碱充分混合,加快反应速率,并使小烧杯内液体温度上下一致.
(2)中和反应放出的热量会造成少量盐酸在反应中挥发,则测得的中和热的数值偏小(填“偏大”、“偏小”或“不变”).
(3)该实验小组做了三次实验,每次取溶液各50mL,并将实验数据记录如表:
已知盐酸、NaOH溶液的密度与水相同,中和后生成的溶液的比热容c=4.18×10-3kJ/(g•℃),则该反应的中和热△H=-56.8 kJ/mol.
(4)在中和热测定实验中,测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热的数值偏小(填“偏大”、“偏小”或“不变”).
 某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)环形玻璃搅拌棒的作用是使酸和碱充分混合,加快反应速率,并使小烧杯内液体温度上下一致.
(2)中和反应放出的热量会造成少量盐酸在反应中挥发,则测得的中和热的数值偏小(填“偏大”、“偏小”或“不变”).
(3)该实验小组做了三次实验,每次取溶液各50mL,并将实验数据记录如表:
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)℃ | 温差(t2-t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.8 | 6.8 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 32.0 | 6.9 |
(4)在中和热测定实验中,测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热的数值偏小(填“偏大”、“偏小”或“不变”).
14.下列与滴定实验有关的说法中正确的是( )
| A. | 容量瓶和滴定管都需要用试剂润洗 | |
| B. | 用NaOH滴定盐酸时,若滴定结束时俯视刻度,会导致测定结果偏高 | |
| C. | 用滴定管准确量取20.0 mL盐酸 | |
| D. | 用KMnO4滴定亚硫酸钠溶液的实验中不需要另外加入指示剂 |
4.2016年10月17日,神州十一号飞船在酒泉卫星发射中心成功发射.根据太空的失重状况,下列化学实验在太空中无法完成的是( )
| A. | 过滤 | B. | 两种固体混合 | ||
| C. | 硫酸与氢氧化钠溶液的中和反应 | D. | 蒸发 |
1.在2L密闭容器中,起始投入2mol N2和3.5mol H2发生反应,测得平衡时的数据如表.若该反应△H<0,则T1<T2(填“>”、“<”或“=”);在温度T2下,若经过10min反应达到平衡,则平均速率v(NH3)=0.05 mol•L-1•min-1,平衡常数为0.33(mol•L-1)-2 (保留两位有效数字)
| 温度 | 平衡时NH3的 物质的量mol |
| T1 | 1.2 |
| T2 | 1.0 |
2.已知甲为恒温恒压容器,乙为恒温恒容容器.初始时,两容器的温度、体积相同,两容器中均充入2molSO2和lmolO2,且发生反应为2SO2(g)+O2(g)?2SO3(g)+Q(Q>0);当两容器都达到平衡后,为使两者中的SO2在平衡混合物中的物质的量分数相同,下列措施中可行的是( )
| A. | 向甲容器中再充人一定量的氦气 | B. | 向乙容器中再充人2mol的SO3气体 | ||
| C. | 适当降低乙容器的温度 | D. | 缩小甲容器的体积 |