题目内容
用单线桥表示下列化学方程式中的电子转移.
(1)2FeCl2+Cl2 ═2FeCl3;
(2)Zn+H2SO4═ZnSO4 +H2 ↑;
(3)H2SO4(浓)+H2S═S↓+SO2 ↑+2H2O;
(4)NH4NO3
N2 O↑+2H2O.
(1)2FeCl2+Cl2 ═2FeCl3;
(2)Zn+H2SO4═ZnSO4 +H2 ↑;
(3)H2SO4(浓)+H2S═S↓+SO2 ↑+2H2O;
(4)NH4NO3
| ||
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)2FeCl2+Cl2 ═2FeCl3中Fe元素化合价由+2价变为+3价、Cl元素化合价由0价变为-1价,转移电子数为2;
(2)Zn+H2SO4═ZnSO4 +H2 ↑中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,转移电子数为2;
(3)H2SO4(浓)+H2S═S↓+SO2 ↑+2H2O中硫酸中S元素化合价由+6价变为+4价、硫化氢中S元素化合价由-2价变为0价,转移电子数为2;
(4)NH4NO3
N2 O↑+2H2O中铵根离子中N元素化合价由-3价变为+1价、硝酸根离子中N元素化合价由+5价变为+1价,转移电子数为4.
(2)Zn+H2SO4═ZnSO4 +H2 ↑中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,转移电子数为2;
(3)H2SO4(浓)+H2S═S↓+SO2 ↑+2H2O中硫酸中S元素化合价由+6价变为+4价、硫化氢中S元素化合价由-2价变为0价,转移电子数为2;
(4)NH4NO3
| ||
解答:
解:(1)2FeCl2+Cl2 ═2FeCl3中Fe元素化合价由+2价变为+3价、Cl元素化合价由0价变为-1价,转移电子数为2,电子转移方向和数目为 ,故答案为:
,故答案为: ;
;
(2)Zn+H2SO4═ZnSO4 +H2 ↑中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,转移电子数为2,电子转移方向和数目为 ,故答案为:
,故答案为: ;
;
(3)H2SO4(浓)+H2S═S↓+SO2 ↑+2H2O中硫酸中S元素化合价由+6价变为+4价、硫化氢中S元素化合价由-2价变为0价,转移电子数为2,电子转移方向和数目为 ,故答案为:
,故答案为: ;
;
(4)NH4NO3
N2 O↑+2H2O中铵根离子中N元素化合价由-3价变为+1价、硝酸根离子中N元素化合价由+5价变为+1价,转移电子数为4,电子转移方向和数目为 ,故答案为:
,故答案为: .
.
 ,故答案为:
,故答案为: ;
;(2)Zn+H2SO4═ZnSO4 +H2 ↑中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,转移电子数为2,电子转移方向和数目为
 ,故答案为:
,故答案为: ;
;(3)H2SO4(浓)+H2S═S↓+SO2 ↑+2H2O中硫酸中S元素化合价由+6价变为+4价、硫化氢中S元素化合价由-2价变为0价,转移电子数为2,电子转移方向和数目为
 ,故答案为:
,故答案为: ;
;(4)NH4NO3
| ||
 ,故答案为:
,故答案为: .
.
点评:本题以电子转移方向和数目的标注为载体考查氧化还原反应,侧重考查计算能力,明确元素化合价变化是解本题关键,注意箭头指向,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以下是几种常用基本物理量的名称与符号的对应关系,其中不正确的是( )
| A、物质的量--mol |
| B、质量--m |
| C、时间--t |
| D、电流--I |
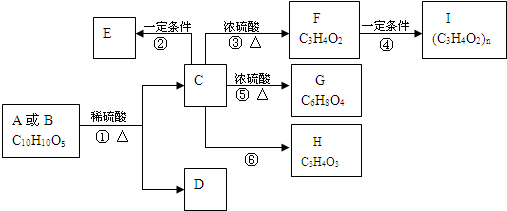
双酚 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:
下列说法正确的是( )
 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:下列说法正确的是( )

| A、1mol双酚A最多可与2mol Br2反应 |
| B、G物质是乙醛的同系物 |
| C、E物质的名称是1-溴丙烷 |
D、反应③的化学方程式是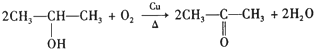 |
乙硼烷常温下一种毒性很大的易燃气体,在近代工业和军事上具有重要用途,主要用于火箭和导弹的高能燃料.0.3mol的高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固体B2O3和液态水,放出649.5KJ的热量.下列关于乙硼烷的叙述正确的是.
| A、B2H6固体时为原子晶体 |
| B、乙硼烷在军事上具有重要用途是因为它有剧毒. |
| C、乙硼烷的燃烧热为2165KJ/mol |
| D、乙硼烷燃烧的热化学方程式为B2H6(g)+3O2(g)═B2O3(S)+3H2O(g)△H=0.165KJ/mol |
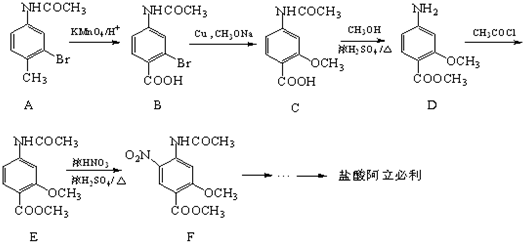
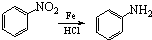 .请写出以
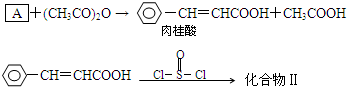
.请写出以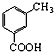 、CH3CH2CH2COCl、CH3OH为原料制备
、CH3CH2CH2COCl、CH3OH为原料制备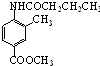 的合成路线流程图(无机试剂任用).合成路线流程图示例如图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如图: .
.

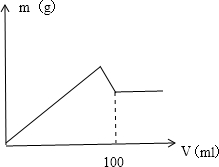 有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.
有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.