题目内容
1.写出下列反应的化学方程式,并注明反应类型.(1)丙烯在催化剂作用下制取聚丙烯:
 [加成反应]
[加成反应](2)乙醇与浓H2SO4加热至170℃制取乙烯:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O[消去反应]
(3)乙醇与O2、Cu共热:2CH3CH2OH+O2$→_{△}^{铜}$2CH3CHO+2H2O[氧化反应]
(4)甲醛(HCHO)与银氨溶液(Ag(NH3)2OH)反应:HCHO+4Ag(NH3)2OH→4Ag↓+2H2O+CO3(NH4)2+6NH3↑[氧化反应]
(5)
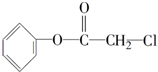 与NaOH溶液共热:
与NaOH溶液共热: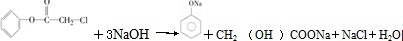 [取代反应].
[取代反应].
分析 (1)丙烯含有碳碳双键,可发生加聚反应生成聚丙烯;
(2)乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯;
(3)乙醇在Cu做催化剂加热时与氧气反应,被氧化生成乙醛和水;
(4)HCHO与足量的银氨溶液反应反应生成碳酸铵、氨气、银和水;
(5) 与NaOH溶液共热,发生酯的水解和卤代烃的消去反应.
与NaOH溶液共热,发生酯的水解和卤代烃的消去反应.
解答 解:(1)丙烯含有碳碳双键,可发生加聚反应生成聚丙烯,反应的方程式为 ,属于加成反应,故答案为:
,属于加成反应,故答案为: ;加成反应;
;加成反应;
(2)乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;消去反应;
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;消去反应;
(3)乙醇在Cu做催化剂加热时与氧气反应,被氧化生成乙醛和水,方程式为2CH3CH2OH+O2$→_{△}^{铜}$2CH3CHO+2H2O,得氧失氢是氧化反应;
故答案为:2CH3CH2OH+O2$→_{△}^{铜}$2CH3CHO+2H2O;氧化反应;
(4)HCHO与足量的银氨溶液反应反应生成碳酸铵、氨气、银和水,化学方程式::HCHO+4Ag(NH3)2OH→4Ag↓+2H2O+CO3(NH4)2+6NH3↑;属于氧化反应,故答案为:HCHO+4Ag(NH3)2OH→4Ag↓+2H2O+CO3(NH4)2+6NH3↑;氧化反应;
(5) 与NaOH溶液共热,发生酯的水解和卤代烃的消去反应,所以反应方程式为:
与NaOH溶液共热,发生酯的水解和卤代烃的消去反应,所以反应方程式为: ,故答案为:
,故答案为: ,取代反应.
,取代反应.
点评 本题考查了化学方程式的书写,明确有机物的结构特点及性质是解题关键,注意反应的条件.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
4.下列关于电解质溶液的正确判断是( )
| A. | 在由水电离产生的C(OH-)=1×10-12 mol•L-1的溶液中,K+、Al3+、SO42-、Cl-一定可以大量共存 | |
| B. | 由0.1 mol/L一元碱BOH溶液的pH=10,可推知BCl溶液呈酸性 | |
| C. | 在pH=0的溶液中,K+、Fe2+、Cl-、NO3-可以大量共存 | |
| D. | 含碳酸氢钠的溶液:K+、SO42-、Cl-、H+能大量共存 |
8.在常温常压下,把1molO2和4molN2混合后占有的体积是( )
| A. | 22.4L | B. | 89.6L | C. | 112L | D. | 大于112L |
13.下列说法正确的是( )
| A. | 卤素元素都有正化合价 | B. | 卤素元素的单质都只具有氧化性 | ||
| C. | 卤素元素的最低化合价都是-1价 | D. | 卤素元素氢化物都是强酸 |
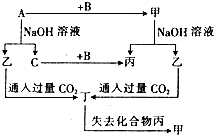 由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题:
由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题: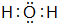 .
. .
.