题目内容
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 将 lmolCl2通入到水中,则n(HClO)+n(Cl-)+n(ClO-)=2NA | |
| B. | 常温常压下,17g甲基(-14CH3)中所含的中子数为9NA | |
| C. | 含NA个阴离子的Na2O2溶于水形成1L溶液,Na+浓度为1 mol•L-1 | |
| D. | 某温度时,1LpH=6.5的纯水中含有1.0×10-6.5NA个H+ |
分析 A.根据氯原子的守恒来分析;
B.1个甲基(-14CH3)含有8个中子;
C.过氧化钠中阴离子为过氧根离子,物质的量浓度中体积为溶液的体积;
D.水的电离程度与温度有关.
解答 解:A.1mol氯气中共含2mol氯原子,而氯气与水的反应为可逆反应,不能进行彻底,故溶液中有HClO分子、ClO-、Cl-、Cl2分子,根据氯原子的守恒可有:2NA=N(HClO)+N(Cl-)+N(ClO-)+2N(Cl2),故A错误;
B.1个甲基(-14CH3)含有8个中子,17g甲基(-14CH3)中所含的中子数为$\frac{17g}{17g/mol}$×8×NA=8NA,故B错误;
C.含NA个阴离子的Na2O2溶于水形成1L溶液,溶液体积大于1L,含有2mol钠离子,Na+浓度小于2 mol•L-1,故C错误;
D.水的电离程度与温度有关,可能在某温度时,1L pH=6的纯水中含有1.0×10-6NA个H+,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大,注意过氧化钠的组成与结构.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
13.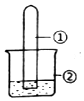 用图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
 用图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测的现象不一致的是( )| 选项 | ①中的物质 | ②中的物质 | 预测装置中现象 |
| A | NO2 | 蒸馏水 | 试管充满无色溶液 |
| B | SO2 | 紫色石蕊溶液 | 溶液逐渐变为红色 |
| C | NH3 | AlCl3溶液 | 产生白色沉淀 |
| D | Cl2 | AgNO3溶液 | 产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
14.X、Y、Z、M为构成生命体的基本元素,其原子序数依次增大,下列说法不正确的是( )
| A. | 四种元素可形成两种以上的盐 | |
| B. | Y、Z、M的氢化物中,M的氢化物最稳定 | |
| C. | 四种元素中原子半径最大的为M | |
| D. | 由四种元素中的两种形成的相对分子质量最小的有机物不能发生加成反应 |
11.下列关于有机化合物的说法正确的是( )
| A. | 乙醇的水溶液俗称酒精 | |
| B. | 由苯与氯气在一定条件下生成C6H6Cl6的反应属于取代反应 | |
| C. | 化学式为C4H10O的饱和一元醇有4种 | |
| D. | 糖类发生水解反应的最终产物都是葡萄糖 |
8.如图为生锈了的家用铁锅,下列有关解释事实的方程式不正确的是( )


| A. | 铁锅生锈过程中有原电池反应,负极反应式是:Fe-2e-=Fe2+ | |
| B. | 铁锅生锈过程中有Fe(OH)3生成:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 用醋可除去铁锈:6CH3COOH+Fe2O3═6CH3COO-+2Fe3++3H2O |
2.下列化学方程式的叙述正确的是( )
| A. | 已知2C(s)+O2(g)=2CO(g)△H=-22lkJ/mol,则C的燃烧热为110.5kJ/mol | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4kJ/mol | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)═2CO(g)△H2 则△H1>△H2 |
19.下列反应中,反应后固体物质增重的是( )
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 氢氧化铝受热分解 | D. | 将锌粒投入CuSO4溶液 |
20.在下列各溶液中,离子不能大量共存的是( )
| A. | 中性溶液中:K+、Fe3+、Cl-、 | |
| B. | Al3+、Cl-、Na+可以大量共存于pH=2的溶液中 | |
| C. | 0.1 mol/L NaAlO2溶液:、Na+、Cl- | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+ |