题目内容
19.下列反应中,反应后固体物质增重的是( )| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 氢氧化铝受热分解 | D. | 将锌粒投入CuSO4溶液 |
分析 A.CuO转化为Cu;
B.过氧化钠转化为碳酸钠;
C.氢氧化铝分解生成氧化铝和水;
D.Zn与CuSO4溶液反应生成ZnSO4、Cu.
解答 解:A.氢气与CuO反应生成Cu和水,CuO固体的质量减小,故A不选;
B.二氧化碳通过Na2O2粉末,反应生成碳酸钠和氧气,固体质量增加,故B选;
C.氢氧化铝分解生成氧化铝和水,氢氧化铝固体质量减小,故C不选;
D.Zn与CuSO4溶液反应生成ZnSO4、Cu,每参加1molZn失去1molCu,溶液质量增加,固体质量减少,故D不选;
故选B.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应、固体质量变化为解答的关键,侧重分析与计算能力的考查,注意判断反应前后的固体,题目难度不大.

练习册系列答案
相关题目
2.下列有关化学用语表示正确的是( )
| A. | 中子数为10的氧原子:${\;}_{8}^{10}$O | B. | Mg2+的结构示意图: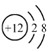 | ||
| C. | 硫化钠的电子式: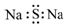 | D. | 氯乙烯的结构简式:C2H3Cl |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 将 lmolCl2通入到水中,则n(HClO)+n(Cl-)+n(ClO-)=2NA | |
| B. | 常温常压下,17g甲基(-14CH3)中所含的中子数为9NA | |
| C. | 含NA个阴离子的Na2O2溶于水形成1L溶液,Na+浓度为1 mol•L-1 | |
| D. | 某温度时,1LpH=6.5的纯水中含有1.0×10-6.5NA个H+ |
7.下列说法不正确的是( )
| A. | 化学反应过程中既有物质变化又有能量变化,能量的释放或吸收以物质变化为基础 | |
| B. | 研究化学反应进行的方向、快慢和限度是化学反应原理的重要内容 | |
| C. | Ag+和Cl-在水溶液中的反应瞬间发生,是因为这类反应活化能接近于零 | |
| D. | 能源就是能提供能量的资源,天然气、风能、水能都是可再生能源 |
14.化学与生产、生活密切相关.下列叙述不正确的是( )
| A. | 煤的气化、液化、干馏均有化学变化 | |
| B. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| C. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| D. | “地沟油”经过加工处理可用来制肥皂 |
4.分子式为C4HCl9的有机物共有(不含立体异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
11.下列说法正确的是( )
| A. | 凡是放热反应都是自发的,吸热反应都是非自发的 | |
| B. | 自发反应的熵一定增大,非自发反应的焓一定减小 | |
| C. | 对于熵增反应,若一定温度下不能自发进行,则该反应的△H>0 | |
| D. | 对于△H>0的反应能自发进行,则该反应的△S<0 |
8.现有某铁的氧化物样品,用35mL5mol•L-1的盐酸恰好完全溶解,向反应后的溶液中通入氯气140mL(标准情况下),Fe2+可以全部转化为Fe3+.则该氧化物的化学式为( )
| A. | Fe2O3 | B. | Fe3O4 | C. | Fe4O5 | D. | Fe5O7 |
9.下列各组离子在给出条件下一定能大量共存的是( )
| A. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 水电离的c(H+)=1.0×10-13mol•L-1的溶液中:Na+、Mg2+、Ca2+、I- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- |