题目内容
19.某无土栽培营养液铭牌如表所示:.若要求KCl、K2SO4 和NH4Cl 三种固体原料的物质的量之比为1:4:8,写出详细的计算过程求出a 和b 的数值分别为( )| 营养液所含成分 | 质量(g) |
| KCl | a |
| K2SO | b |
| NH4Cl | 428 |
| A. | 53.5 和214 | B. | 74.5 和348 | C. | 74.5 和696 | D. | 149 和696 |
分析 由428gNH4Cl可计算其物质的量,再由NH4Cl、K2SO4、KCl三种固体原料的物质的量之比为8:4:1,可计算KCl和K2SO4的物质的量,利用m=nM来计算它们的质量.
解答 解:428gNH4Cl的物质的量为:$\frac{428g}{53.5g/mol}$=8mol,
由NH4Cl、K2SO4、KCl三种固体原料的物质的量之比为8:4:1可知,
则KCl的物质的量为1mol,其质量为:1mol×74.5g/mol=74.5g,即a=74.5;
K2SO4的物质的量为4mol,其质量为:4mol×174g/mol=696g,即b=696,
故选C.
点评 本题考查物质的量的计算,为高频考点,题目难度不大,侧重于学生的分析能力和计算能力的考查,明确质量、物质的量的关系即可解答.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
19.下列说法中错误的是( )
| A. | HCl、HBr、HI、HF的沸点依次升高 | |
| B. | 氨分子中N-H键的极性小于水分子中O-H键的极性 | |
| C. | 乙醇分子间存在氢键,乙醛分子间不存在氢键,故乙醇的沸点高于乙醛 | |
| D. | 由于N-H键强于P-H键,故NH3的沸点高于PH3 |
10.已知:298K时,2SO2(g)+O2(g)?2SO3(g);△H=-Q1 KJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q2KJ,则下列关系式正确的是( )
| A. | 无法比较 | B. | Q1<Q2 | C. | Q1=Q2 | D. | Q1>Q2 |
9.阅读、分析下列两个材料:
材料一、如图
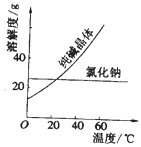
材料二
回答下列问题:
(1)要从氯化钠和纯碱的固体混合物中分离得到纯净的氯化钠,应先将固体溶解,再经过蒸发结晶趁热过滤、洗涤、干燥等操作.
(2)将乙二醇和丙三醇相互分离的最佳方法是蒸馏法,写出该方法在操作上的注意事项(写出一项)蒸馏烧瓶中应加入沸石.
材料一、如图

材料二
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
(1)要从氯化钠和纯碱的固体混合物中分离得到纯净的氯化钠,应先将固体溶解,再经过蒸发结晶趁热过滤、洗涤、干燥等操作.
(2)将乙二醇和丙三醇相互分离的最佳方法是蒸馏法,写出该方法在操作上的注意事项(写出一项)蒸馏烧瓶中应加入沸石.
 用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )