题目内容
16.分离下列混合物,按溶解、过滤、蒸发顺序进行的是( )| A. | 碳酸钙、木炭 | B. | 氧化铜、硝酸钾 | C. | 乙醇、碘 | D. | 硝酸钾、氯化钠 |
分析 按溶解、过滤、蒸发顺序分离混合物,则其中一种不溶于水,一种可溶于水,结合物质的溶解性来解答.
解答 解:A.二者均不溶于水,过滤不能分离,故A不选;
B.CuO不溶于水,硝酸钾溶于水,则可按溶解、过滤、蒸发顺序分离,故B选;
C.二者均溶于水,不能过滤分离,故C不选;
D.二者均溶于水,不能过滤分离,故D不选;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
6.下列物质中,属于强电解质的是( )•
| A. | NH3•H2O | B. | BaSO4 | C. | 蔗糖 | D. | 稀硫酸 |
7.做化学实验时,必须十分重视安全和环保问题.下列操作方法不符合上述要求的是( )
| A. | 钠、镁等金属着火,不可用CO2灭火 | |
| B. | 在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度 | |
| C. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| D. | 给试管中的液体加热时,不停沿试管倾斜方向移动试管或加入碎瓷片,以免液体暴沸伤人 |
4.下列说法正确的是( )
| A. | 32g氧气和臭氧混合物中氧原子的物质的量为2 mol | |
| B. | 2mol的硫酸的摩尔质量为196g/mol | |
| C. | 一定温度和压强下,各种气态物质的体积由构成气体分子的大小决定 | |
| D. | 将58.5gNaCl溶于941.5g水中配成1mol/L的NaCl溶液 |
1.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L氢气中含有2NA个中子 | |
| B. | 0.1NA个氯化氢分子占有体积为2.24L | |
| C. | 2克金属钙变成钙离子时失去的电子数为0.1NA | |
| D. | 50mL0.1mol/L H2SO4溶液中含有H+数为0.005NA |
8.下列过程或现象与盐类水解无关的是( )
| A. | NaX溶液的pH>7,则可证明HX属于弱电解质 | |
| B. | 二氯化铁溶液可以做电子工业中铜版的刻蚀液 | |
| C. | 实验室盛放NaF溶液不能用玻璃材质的试剂瓶及玻璃塞 | |
| D. | 浓的硫化钠溶液有强烈的臭味 |
5.下列实验操作能够达到实验目的是( )
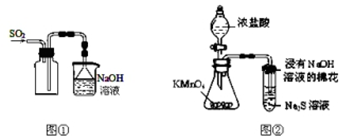

| A. | 实验室采用图①所示装置收集SO2 | |
| B. | 除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 | |
| C. | 称取0.40 g NaOH,置于100 mL容量瓶中,加水溶解,配制0.10 mol/L NaOH溶液 | |
| D. | 可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱 |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1L lmol•L-1 FeBr2溶液与l molCl2反应时转移的电子数目为3NA | |
| B. | 7g分子式为CnH2n的链烃中含有的C-H键的数目为NA | |
| C. | 常温时,1.0L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | 0.5mol•L-1硫酸钠溶液中含有溶质离子总数为1.5NA |
 .
.