题目内容
常温下,在47.9g水中溶解12.1g Cu(NO3)2?3H2O,恰好达到饱和,设该溶液密度为1.20g/cm3,求:
(1)该溶液中Cu(NO3)2的物质的量;
(2)溶液的体积;
(3)该溶液中Cu(NO3)2的物质的量浓度;
(4)取出20.0ml该溶液,配成浓度为0.2mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
(1)该溶液中Cu(NO3)2的物质的量;
(2)溶液的体积;
(3)该溶液中Cu(NO3)2的物质的量浓度;
(4)取出20.0ml该溶液,配成浓度为0.2mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
考点:物质的量浓度的相关计算
专题:计算题
分析:(1)根据n=
来计算;
(2)根据V=
来计算;
(3)根据C=
来计算;
(4)根据溶液的稀释定律C浓V浓=C稀V稀来计算.
| m |
| M |
(2)根据V=
| m |
| ρ |
(3)根据C=
| n |
| V |
(4)根据溶液的稀释定律C浓V浓=C稀V稀来计算.
解答:
解:(1)由分析知,Cu(NO3)2?3H2O的物质的量n=
=
=0.05mol,
根据1molCu(NO3)2?3H2O~1molCu(NO3)2,故Cu(NO3)2的物质的量n=0.05mol,
答:该溶液中Cu(NO3)2的物质的量为0.05mol;
(2)由分析知,溶液的体积V=
=
=50ml
答:溶液的体积为50ml;
(3)由分析知,溶液中Cu(NO3)2的物质的量浓度C=
=
=1mol/L
答:溶液中Cu(NO3)2的物质的量浓度为1mol/L;
(4)设稀释后溶液的体积是VL,根据稀释定律C浓V浓=C稀V稀可知:
1mol/L×0.02L=0.2mol/L×VL
解得:V=0.1L=100ml,
答:稀释后溶液的体积是100ml.
| m |
| M |
| 12.1g |
| 242g/mol |
根据1molCu(NO3)2?3H2O~1molCu(NO3)2,故Cu(NO3)2的物质的量n=0.05mol,
答:该溶液中Cu(NO3)2的物质的量为0.05mol;
(2)由分析知,溶液的体积V=
| m |
| ρ |
| 47.9g+12.1g |
| 1.20g/cm3 |
答:溶液的体积为50ml;
(3)由分析知,溶液中Cu(NO3)2的物质的量浓度C=
| n |
| V |
| 0.05mol |
| 0.05L |
答:溶液中Cu(NO3)2的物质的量浓度为1mol/L;
(4)设稀释后溶液的体积是VL,根据稀释定律C浓V浓=C稀V稀可知:
1mol/L×0.02L=0.2mol/L×VL
解得:V=0.1L=100ml,
答:稀释后溶液的体积是100ml.
点评:本题考查了配制溶液时物质的量浓度的计算、溶液体积的计算以及溶液的稀释,熟悉公式的使用是关键,难度不大.

练习册系列答案
相关题目
现有两种只含C、H两种元素的有机物混合气体0.1mol,完全燃烧生成0.12molCO2和0.2molH2O,则该混合气体中( )
| A、一定含有甲烷 |
| B、一定含有乙烯 |
| C、可能含有甲烷 |
| D、不能确定 |
 ,这是21世纪具有广阔前景的合成材料.
,这是21世纪具有广阔前景的合成材料.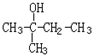 此化合物在浓硫酸作用下发生消去反应,写出所有可能的有机产物的结构简式:
此化合物在浓硫酸作用下发生消去反应,写出所有可能的有机产物的结构简式: