题目内容
分析下列溶液蒸干后得到的固体是什么?写出其化学式:
(1)K2CO3溶液蒸干得到的固体物质是 .
(2)(NH4)2SO4溶液蒸干得到的固体物质是 .
(3)Ba(HCO3)2溶液蒸干得到的固体物质是 .
(4)Na2SO4溶液蒸干得到的固体物质是 .
(5)Mg(HCO3)2溶液蒸干得到的固体物质是 .
(1)K2CO3溶液蒸干得到的固体物质是
(2)(NH4)2SO4溶液蒸干得到的固体物质是
(3)Ba(HCO3)2溶液蒸干得到的固体物质是
(4)Na2SO4溶液蒸干得到的固体物质是
(5)Mg(HCO3)2溶液蒸干得到的固体物质是
考点:盐类水解的应用
专题:盐类的水解专题
分析:易水解的盐,若水解生成强碱或难挥发性强酸,则蒸干其溶液得到原物质,若水解生成易挥发性的酸,则蒸干其溶液得到氢氧化物;碳酸氢盐受热易分解,蒸干得到碳酸盐,Mg(HCO3)2在溶液中水解生成氢氧化镁据此分析.
解答:
解:(1)K2CO3在溶液中水解生成强碱KOH和KHCO3,浓度增大时二者又重新生成K2CO3,则蒸干得到的固体物质是K2CO3;
故答案为:K2CO3;
(2)(NH4)2SO4在溶液中水解生成难挥发性强酸硫酸和NH4HSO4,浓度增大时二者又重新生成(NH4)2SO4,则蒸干得到的固体物质是(NH4)2SO4;
故答案为:(NH4)2SO4;
(3)Ba(HCO3)2受热易分解,溶液蒸干得到的碳酸盐BaCO3,故答案为:BaCO3;
(4)Na2SO4属于强酸强碱盐,在溶液中不水解,也不易分解,所以液蒸干得到的固体物质是Na2SO4;故答案为:Na2SO4;
(5)Mg(HCO3)2在溶液中水解生成氢氧化镁,所以Mg(HCO3)2溶液蒸干得到的固体物质是Mg(OH)2,故答案为:Mg(OH)2.
故答案为:K2CO3;
(2)(NH4)2SO4在溶液中水解生成难挥发性强酸硫酸和NH4HSO4,浓度增大时二者又重新生成(NH4)2SO4,则蒸干得到的固体物质是(NH4)2SO4;
故答案为:(NH4)2SO4;
(3)Ba(HCO3)2受热易分解,溶液蒸干得到的碳酸盐BaCO3,故答案为:BaCO3;
(4)Na2SO4属于强酸强碱盐,在溶液中不水解,也不易分解,所以液蒸干得到的固体物质是Na2SO4;故答案为:Na2SO4;
(5)Mg(HCO3)2在溶液中水解生成氢氧化镁,所以Mg(HCO3)2溶液蒸干得到的固体物质是Mg(OH)2,故答案为:Mg(OH)2.
点评:本题考查了盐类水解,明确盐的水解规律是解本题关键,注意碳酸氢盐易分解、Mg(HCO3)2易水解生成Mg(OH)2,题目难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
将a mL NO,b mL NO2和c mL O2混合于同一试管中,将试管倒置于水中,充分反应后,试管内气体全部消失,则a:b:c不可能是( )
| A、1:1:1 |
| B、2:1:1 |
| C、3:4:7 |
| D、1:5:2 |
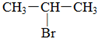 ;1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如图所示的一系列变化.
;1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如图所示的一系列变化.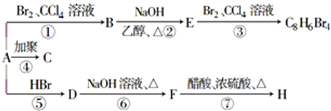
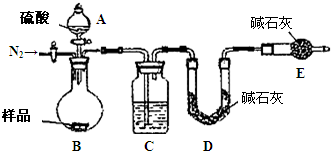 纯碱是工业生产和日常生活中的重要物质.某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列四种实验方案进行探究.请填空:
纯碱是工业生产和日常生活中的重要物质.某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列四种实验方案进行探究.请填空: