题目内容
碱式碳酸铜和氯气都是用途广泛的化工原料.
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
①氯酸钠的作用是 ;
②反应A后调节溶液的pH范围应为 .
③第一次过滤得到的产品洗涤时,如何判断已经洗净? .
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
②反应A后调节溶液的pH范围应为
③第一次过滤得到的产品洗涤时,如何判断已经洗净?
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:由流程图可知:刻蚀废液加入NaClO3把亚铁离子氧化为铁离子,调节PH除掉铁离子,滤渣为Fe(OH)3,向CuCl2溶液中加入碳酸钠固体,过滤得到碱式碳酸铜.
①工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,流程分析,加入氯酸钠的作用是氧化剂作用,氧化亚铁离子为铁离子易于除去;
②依据图表数据分析,铁离子全部沉淀,铜离子不沉淀的PH范围为3.2-4.2;
③检验洗涤是否干净,设计实验检验滤液中是否含有氯离子证明是否洗涤干净.
①工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,流程分析,加入氯酸钠的作用是氧化剂作用,氧化亚铁离子为铁离子易于除去;
②依据图表数据分析,铁离子全部沉淀,铜离子不沉淀的PH范围为3.2-4.2;
③检验洗涤是否干净,设计实验检验滤液中是否含有氯离子证明是否洗涤干净.
解答:
解:①工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备碱式碳酸铜,流程分析,加入氯酸钠的作用是氧化剂作用,氧化亚铁离子为铁离子,调节溶液PH易于把铁离子沉淀除去,
故答案为:将Fe2+氧化成Fe3+并最终除去;
②流程分析可知,分离除杂的方法是通过调节溶液PH大于3.2,小于4.2,使铁离子全部沉淀完全,铜离子不沉淀,达到分离的目的,
故答案为:3.2-4.2;
③沉淀表面会含有氯化钠溶液,设计实验检验是否含有氯离子的方法可以检验是否洗涤干净,实验设计为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净,故答案为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
故答案为:将Fe2+氧化成Fe3+并最终除去;
②流程分析可知,分离除杂的方法是通过调节溶液PH大于3.2,小于4.2,使铁离子全部沉淀完全,铜离子不沉淀,达到分离的目的,
故答案为:3.2-4.2;
③沉淀表面会含有氯化钠溶液,设计实验检验是否含有氯离子的方法可以检验是否洗涤干净,实验设计为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净,故答案为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
点评:本题考查了实验探究物质分离方法和物质性质的分析判断,为高频考点,侧重学生的分析能力和实验能力的考查,注意实验室制备气体的过程分析和氯气性质的应用判断,题目难度中等.

练习册系列答案
相关题目
 如图是两组物质之间在一定的条件下相互转化的过程.下列绿色植物通过光合作用说法不正确的是( )
如图是两组物质之间在一定的条件下相互转化的过程.下列绿色植物通过光合作用说法不正确的是( )| A、物质X是O2 |
| B、绿色植物通过光合作用,将太阳能转化成化学能 |
| C、C6H12O6是碳氢氧三种元素组成的化合物 |
| D、C6H12O6与X反应生成CO2和H2O属于置换反应 |
 如图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是( )
如图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是( )| A、B中收集到的气体是氢气 |
| B、烧杯中双氧水溶液作用是将Fe2+还原为Fe3+ |
| C、A中的氧化铁与盐酸反应生成氯化铁 |
| D、烧杯中溶液在氯化氢气氛下,蒸发浓缩、冷却结晶、过滤后得到氯化铁晶体 |
下列说法正确的是( )
| A、用丙酮与盐酸的混合液作展开剂,对Fe3+与Cu2+用纸层析法分离时,Fe3+移动较快 |
| B、阿司匹林制备实验中,将粗产品加入饱和NaOH溶液中以除去水杨酸聚合物 |
| C、用瓷坩锅高温熔融NaOH和Na2CO3的固体混合物 |
| D、标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
固体硝酸盐加热易分解且产物较复杂.某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想,其中不成立的是( )
| A、Mg、NO2、O2 |
| B、MgO、NO2、O2 |
| C、Mg3N2、O2 |
| D、MgO、NO2、N2 |
 已知A与B相互转化:2A(g)?B(g);△H=-24.4J/mol.在恒温下,将一定量的A和B混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图,下列推断合理的是( )
已知A与B相互转化:2A(g)?B(g);△H=-24.4J/mol.在恒温下,将一定量的A和B混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图,下列推断合理的是( )| A、前10min内,用v(A)为0.02mol/(L?min) |
| B、反应进行前10min时,体系吸收热量9.76kJ |
| C、b、c、d三点中反应速率d>b=c |
| D、25min时,导致平衡移动的原因是升温 |
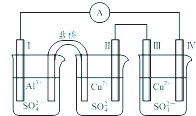 某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其它均为Cu电极,则下列叙述正确的是( )
某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其它均为Cu电极,则下列叙述正确的是( )| A、电子流动方向:电极Ⅳ→A→电极Ⅰ |
| B、电极Ⅰ发生氧化反应 |
| C、电极Ⅱ质量不变 |
| D、电极Ⅲ的电极反应:Cu2++2e-=Cu |
 实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)?NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵.
实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)?NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵.