题目内容
5.下列有关化学用语正确的是( )| A. | NaOH的电子式: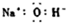 | B. | I4O9(碘酸碘)中碘的化合价为+3,+5 | ||
| C. | NH5的结构式为: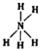 | D. | CO2的比例模型: |
分析 A、氢氧化钠是由钠离子和氢氧根构成的;
B、根据名称可知,I4O9中含碘酸根(IO3-),且根据氧原子个数可知,含有的碘酸根的为3个;
C、NH5为离子化合物,由铵根离子和H-构成;
D、二氧化碳分子为直线型结构.
解答 解:A、氢氧化钠属于离子化合物,电子式中需要标出阴阳离子所带电荷,钠离子直接用离子符号表示,氢氧根离子需要标出最外层电子,氢氧化钠的电子式为: ,故A错误;
,故A错误;
B、根据名称可知,I4O9中含碘酸根(IO3-),且根据氧原子个数可知,含有的碘酸根的为3个,故I4O9可以写成I(IO3)3的形式,故碘元素的价态有+3价和+5价,故B正确;
C、NH5为离子化合物,由铵根离子和H-构成,故无结构式,故C错误;
D、二氧化碳分子为直线型结构,三个原子在一条直线上,不存在夹角,故应为 ,故D错误.
,故D错误.
故选B.
点评 本题考查常用化学用语,难度不大,加强基础知识的掌握理解,注意C选项容易受化学式的书写影响.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
15.工业上制取CuSO4不是直接用铜和浓硫酸反应,而是将铜和少量银的混合物浸在稀硫酸中,并不断从容器底部吹入细小的空气泡.这样做的优点是( )
①不产生污染大气的SO2 ②提高硫酸的利用率 ③节省能源 ④提高铜的利用率.
①不产生污染大气的SO2 ②提高硫酸的利用率 ③节省能源 ④提高铜的利用率.
| A. | ②③ | B. | ①④ | C. | ①②③ | D. | ①② |
13.H2S是一种有臭鸡蛋气味的气体,其分子结构和H2O相似,但S-H键键能比O-H键键能低.下列判断错误的是( )
| A. | H2S分子呈V形 | |
| B. | H2S沸点低于H2O沸点,因为S-H键键能低 | |
| C. | H2S分子中只含σ键 | |
| D. | H2S分子稳定性低于H2O分子,因为O-H键键能高 |
20.某烃不与溴水反应,能使酸性高锰酸钾溶液褪色,在Fe存在下与Cl2反应,能生成两种一氯代物,该烃是( )
| A. | 丙烯 | B. | 对二甲苯 | C. | 1-甲基-4-乙基苯 | D. | 1-甲基-2-乙基苯 |
10.通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知部分化学键的键能如下:
(1)发射神舟飞船的长征火箭用了肼(N2H4,气态)为燃料,若它在氧气(气态)中燃烧,生成N2(气态)和H2O(液态).1mol肼完全燃烧时放出的热量为577kJ.
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH 溶液.肼-空气燃料电池放电时,正极的电极反应式是O2+2H2O+4e-=4OH-.
(3)已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有90个N-N键.
| 化学键 | N-H | N-N | O═O | N≡N | O-H |
| 键能 (kJ•mol-1) | 386 | 167 | 498 | 946 | 460 |
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH 溶液.肼-空气燃料电池放电时,正极的电极反应式是O2+2H2O+4e-=4OH-.
(3)已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有90个N-N键.
17.用如图所示装置进行喷泉实验,烧瓶中充满的气体是( )
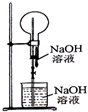

| A. | HCl | B. | CH4 | C. | N2 | D. | NO |
17.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )
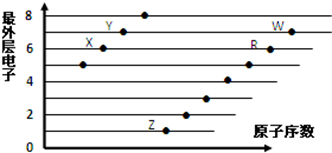

| A. | X和R在同一周期 | |
| B. | 原子半径:W>R>X | |
| C. | 气态氢化物的酸性:X>Y | |
| D. | X、Z形成的化合物中阴阳离子个数比为1:2 |