题目内容
最近有研究人员发现了一种处理高浓度乙醛废水的新方法—隔膜电解法,乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸。实验室以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如右图所示。下列说法不正确的是
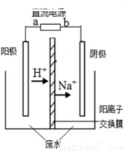
A.若以CH4—空气燃料电池为直流电源,燃料电池的a极应通入空气
B.阳极反应CH3CHO -2e- + H2O = CH3COOH +2H+
C.电解过程中,阴极区Na2SO4的物质的量增大
D.电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2
C
【解析】
试题分析:A.若以CH4—空气燃料电池为直流电源,由于a电极是阳极,所以燃料电池的a极应通入空气,b极通入燃料甲烷,正确;B.乙醛在阳极发生氧化反应产生乙酸,阳极反应CH3CHO -2e- + H2O =CH3COOH +2H+,C.电解过程中,Na2SO4电离产生的离子在两个电极都不发生反应,故其物质的量不变。错误。D. 电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2,阴极产生H2。正确。
考点:考查电化学反应在处理乙醛废水中的应用的知识。

练习册系列答案
相关题目


 在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) 。
在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) 。 的同分异构体很多,其中符合下列条件有______种。
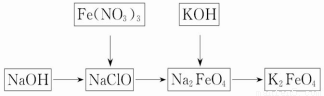
的同分异构体很多,其中符合下列条件有______种。 是一种建筑材料,根据题中合成路线信息,以甲苯为原料合成该高分子化合物,请设计合成路线(无机试剂及溶剂任选)。注:合成路线的书写格式参照如下示例流程图:
是一种建筑材料,根据题中合成路线信息,以甲苯为原料合成该高分子化合物,请设计合成路线(无机试剂及溶剂任选)。注:合成路线的书写格式参照如下示例流程图: