��Ŀ����
2011��3�£��ձ�����9�����𣬵���������Х�������������ؽ����ٶ������ѣ�������ˮ��ȫ����Ҫ����֮һ�����������һ����Ҫ����ɫ��ˮ�������о�ˮ������˫�ع��ܡ�ij����ѧϰС��������·����Ʊ�������أ�
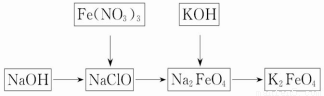
��1�������������Ԫ�صĻ��ϼ�Ϊ_______�ۣ��Ʋ������еĻ�ѧ������____ __��
��2���ڴ�������(NaClO��84����Һ����Ҫ�ɷ�)��Һ�м����ռ�����γɼ��Ի���������ĥ��������������εؼ��뵽������Һ�У���ԡ�з�Ӧ1h�����������ӷ�ӦΪ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O����������________����KOH���뵽��Ӧ�����Һ�����Сʱ�����ã����˴ֲ�Ʒ���÷�Ӧ�Ļ�ѧ����ʽΪ2KOH+Na2FeO4====K2FeO4+2NaOH�����ݸ��ֽⷴӦԭ�����������Ƶ��ܽ��________������ص��ܽ��(����ڡ�����С�ڡ����ڡ�)��
��3����ǿ������Һ�У���������ܽ��Ǹ�����(KCrO2)����Ϊ������(K2CrO4)�����ɵĸ�������Һ�ữ�õ����ظ����(K2Cr2O7)��Fe(��)�ı���Һ�ζ����Զ�����������Ϊָʾ��������ζ��յ�ʱ����Һ����ɫ��Ϊ����ɫ(+6�۸�ת����+3�۸�)���й����ӷ���ʽΪFeO42-+CrO2-+2H2O====CrO42-+Fe(OH)3��+OH-��2CrO42-+2H+====Cr2O72-+H2O��Cr2O72-+6Fe2++14H+====2Cr3++6Fe3++7H2O
�ֳ�ȡ5.00 g���������Ʒ���ձ��У�������������������Һ�������Թ�����KCrO2����ַ�Ӧ��ת�Ƶ�250 mL����ƿ�У����ݣ���ȡ25.00 mL������ϡ�����ữ����0.100 0 mol��L-1��(NH4)2Fe(SO4)2����Һ�ζ�����ȥ����Һ30.00 mL����������ʵ���Ƶõ���Ʒ�У�������ص���������Ϊ__________��
��10�֣���1��+6 ǿ������ ��2���������� ���� ��3��39.6%
��������
�����������1��������صĻ�ѧʽΪK2FeO4�����ݻ�ѧʽ�л��ϼ۵Ĵ�����Ϊ0�ɵ�FeԪ�صĻ��ϼ�Ϊ+6�����������FeԪ�ش�����ۣ��������ؾ���ǿ�����ԡ�
��2������2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O�л��ϼ۵ı仯��ClO?��ClԪ����+1�۽���ΪCl?�еġ�1�ۣ�����������Ϊ�������ƣ����ݸ��ֽⷴӦԭ������Ӧ������ܵķ�����У�2KOH+Na2FeO4=K2FeO4+2NaOH�����Ը������Ƶ��ܽ�ȴ��ڸ�����ص��ܽ�ȡ�
��3���������ӷ���ʽFeO42-+CrO2-+2H2O=CrO42-+Fe(OH)3��+OH-��2CrO42-+2H+=Cr2O72-+H2O��Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O�ɵö�Ӧ��ϵ��2FeO42?��2CrO2-��Cr2O72?��6Fe3+���ɵ�FeO42?��3Fe2+����25.00 mL ��Һ��n��FeO42?��=1/3n��Fe2+��=1/3��0.100 0 mol��L-1��0.03L=0.001mol����25oml�к�FeO42?���ʵ���Ϊ0.01mol�����Ը�����ص���������=0.01mol��198g/mol��5g��100%=39.6%��
���㣺���⿼��������ԭ��Ӧԭ�������ֽⷴӦ����ѧ���㡣

 2C3��g������H ����a kJ/mol��a��0������һ���д����Ĺ̶��ݻ��������м���2 mol A2��1 mol B2����500 ��ʱ��ַ�Ӧ��ƽ���C3��Ũ��Ϊw mol/L���ų�����b kJ��
2C3��g������H ����a kJ/mol��a��0������һ���д����Ĺ̶��ݻ��������м���2 mol A2��1 mol B2����500 ��ʱ��ַ�Ӧ��ƽ���C3��Ũ��Ϊw mol/L���ų�����b kJ��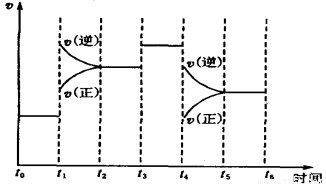
 2CO��g��������Ӧ���ȣ�������Ӧ����Ϊv1��N2(g)+3H2(g)
2CO��g��������Ӧ���ȣ�������Ӧ����Ϊv1��N2(g)+3H2(g) 2C+2D,��4�ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��λmol��L��1��s��1��
2C+2D,��4�ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��λmol��L��1��s��1��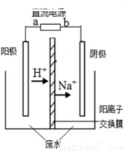
 2G(g)�����Թ��������ƽ��ʱG���������(%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��
2G(g)�����Թ��������ƽ��ʱG���������(%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��