题目内容
某有机物A,由C、H、O三种元素组成,在一定条件下,由A可以转化为有机物B、C和D、E;C又可以转化为B、A.它们的转化关系如下:

已知D的蒸气密度是氢气的22倍,并可以发生银镜反应.
(1)写出A、B、C、D、E、F的结构简式和名称;
(2)写出实现①②③④⑤⑥⑦⑧转化的化学方程式,并注明反应类型.

已知D的蒸气密度是氢气的22倍,并可以发生银镜反应.
(1)写出A、B、C、D、E、F的结构简式和名称;
(2)写出实现①②③④⑤⑥⑦⑧转化的化学方程式,并注明反应类型.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:D的蒸气密度是氢气的22倍,则相对分子质量为44,并可以发生银镜反应,说明含有-CHO,则D为CH3CHO,由转化关系可知E为CH3COOH,A为CH3CH2OH,B为CH2=CH2,C为CH3CH2Br,则F为CH3COOC2H5,结合有机物的性质以及官能团的变化解答该题.
解答:
解:D的蒸气密度是氢气的22倍,则相对分子质量为44,并可以发生银镜反应,说明含有-CHO,则D为CH3CHO,由转化关系可知E为CH3COOH,A为CH3CH2OH,B为CH2=CH2,C为CH3CH2Br,则F为CH3COOC2H5,
(1)由以上分析可知,A为CH3CH2OH,名称为乙醇,B为CH2=CH2,名称为乙烯,C为CH3CH2Br,名称为溴乙烷,D为CH3CHO,名称为乙醛,E为CH3COOH,名称为乙酸,F为CH3COOC2H5,名称为乙酸乙酯,
故答案为:CH3CH2OH,乙醇;CH2=CH2,乙烯;CH3CH2Br,溴乙烷;CH3CHO,乙醛;CH3COOH,乙酸;CH3COOC2H5,乙酸乙酯;
(2)反应①是乙醇脱水生成乙烯,反应方程式为CH3CH2OH
CH2=CH2↑+H2O,是消去反应,
反应②是乙烯与溴化氢加成生成溴乙烷,反应方程式为CH2=CH2+HBr=CH3CH2Br,是加成反应,
反应③是溴乙烷发生消去反应生成乙烯,反应方程式为:CH3CH2Br+NaOH
CH2=CH2+NaBr+H2O,是消去反应,
反应④是溴乙烷碱性水解得乙醇,反应方程式为CH3CH2Br+NaOH
CH3CH2OH+NaBr,是取代反应,
反应⑤是乙醇氧化生成乙醛,反应方程式为2CH3CH2OH+O2
2CH3CHO+2H2O,是氧化反应,
反应⑥是乙醛氧化成乙酸,反应方程式为2CH3CHO+O2
2CH3COOH,是氧化反应,
反应⑦是乙醛发生还原反应生成乙醇,反应方程式为:CH3CHO+H2
CH3CH2OH,是加成反应,
反应⑧是乙酸与乙醇反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O,是取代反应,
故答案为:CH3CH2OH
CH2=CH2↑+H2O,是消去反应;CH2=CH2+HBr=CH3CH2Br,是加成反应;CH3CH2Br+NaOH
CH2=CH2+NaBr+H2O,是消去反应;CH3CH2Br+NaOH
CH3CH2OH+NaBr,是取代反应;2CH3CH2OH+O2
2CH3CHO+2H2O,是氧化反应;2CH3CHO+O2
2CH3COOH,是氧化反应;CH3CHO+H2
CH3CH2OH,是加成反应;CH3COOH+CH3CH2OH
CH3COOC2H5+H2O,是取代反应.
(1)由以上分析可知,A为CH3CH2OH,名称为乙醇,B为CH2=CH2,名称为乙烯,C为CH3CH2Br,名称为溴乙烷,D为CH3CHO,名称为乙醛,E为CH3COOH,名称为乙酸,F为CH3COOC2H5,名称为乙酸乙酯,
故答案为:CH3CH2OH,乙醇;CH2=CH2,乙烯;CH3CH2Br,溴乙烷;CH3CHO,乙醛;CH3COOH,乙酸;CH3COOC2H5,乙酸乙酯;
(2)反应①是乙醇脱水生成乙烯,反应方程式为CH3CH2OH
| 浓硫酸 |
| 170℃ |
反应②是乙烯与溴化氢加成生成溴乙烷,反应方程式为CH2=CH2+HBr=CH3CH2Br,是加成反应,
反应③是溴乙烷发生消去反应生成乙烯,反应方程式为:CH3CH2Br+NaOH
| 醇 |
| △ |
反应④是溴乙烷碱性水解得乙醇,反应方程式为CH3CH2Br+NaOH
| 水 |
| △ |
反应⑤是乙醇氧化生成乙醛,反应方程式为2CH3CH2OH+O2
| 催化剂 |
反应⑥是乙醛氧化成乙酸,反应方程式为2CH3CHO+O2
| 催化剂 |
反应⑦是乙醛发生还原反应生成乙醇,反应方程式为:CH3CHO+H2
| 催化剂 |
反应⑧是乙酸与乙醇反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:CH3CH2OH
| 浓硫酸 |
| 170℃ |
| 醇 |
| △ |
| 水 |
| △ |
| 催化剂 |
| 催化剂 |
| 催化剂 |
| 浓硫酸 |
| △ |
点评:本题考查有机物的推断,题目难度不大,本题注意以D为解答该题的突破口,结合物质反应的体积判断物质的种类.把握有机物官能团的结构和性质是解答该类题目的关键.

练习册系列答案
相关题目
下列有实验装置的说法,正确的是( )
A、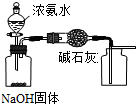 用装置制取干燥纯净的NH3 |
B、 用装置制备Fe(OH)2并能较长时间观察其颜色 |
C、 装置可证明非金属性Cl>C>Si |
D、 装置向左推动针筒活塞可检验该装置的气密性 |
某有机物的结构简式如图所示,下列有关该有机物的说法中正确的是( )


| A、能和碳酸钠溶液反应的官能团有2种 |
| B、1mol该有机物最多能与2molH2发生加成 |
C、与 互为同分异构体 互为同分异构体 |
| D、既可以发生取代反应又可以发生氧化反应 |
下列各组物质相互反应后,最终没有白色沉淀生成的是( )
| A、过量Ba( OH)2溶液加入明矾溶液 |
| B、过氧化钠投入到FeC12溶液中 |
| C、向NaAlO2溶液中通入过量CO2 |
| D、向饱和Na2CO3溶液中通入过量CO2 |
 常温下,向20mL 0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液,有关微粒的物质的量变化如图,(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液,有关微粒的物质的量变化如图,(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)根据图示判断,下列说法正确的是( )| A、H2A在水中的电离方程式是:H2A=H++HA-、HA-?H++A2- |
| B、当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2- )>c(OH-) |
| C、等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度一定比纯水大 |
| D、当V(NaOH)=30mL时,溶液中存在以下关系:c(H+)+c(HA-)+2c(H2A)=c(OH-) |
水的电离平衡曲线如图所示,下列说法中,正确的是( )


| A、图中A、B、D三点处Kw的大小关系:B>A>D |
| B、25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中c(NH4+)/c(NH3?H2O)的值逐渐减小 |
| C、在25℃时,保持温度不变,在水中加人适量NH4Cl固体,体系可从A点变化到C点 |
| D、A点所对应的溶液中,可同时大量存在Na+、Fe3+、Cl-、S042- |

