题目内容
25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
| A、C(s)+12O2(g)=CO(g)△H=-393.5 kJ/mol |
| B、2H2(g)+O2(g)=2H2O(l)△H=+571.6 kJ/mol |
| C、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ/mol |
| D、C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H=-2800 kJ/mol |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,H生成液态水,C生成二氧化碳,据此分析判断.
解答:
解:燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,H生成液态水,C生成二氧化碳,
A、反应中生成一氧化碳不是稳定氧化物,故A错误;
B、氢气燃烧是放热反应,故B错误;
C、生成物水是气体不是稳定氧化物,故C错误;
D、符合燃烧热的概念,故D正确;
故选D.
A、反应中生成一氧化碳不是稳定氧化物,故A错误;
B、氢气燃烧是放热反应,故B错误;
C、生成物水是气体不是稳定氧化物,故C错误;
D、符合燃烧热的概念,故D正确;
故选D.
点评:本题考查了燃烧热的概念分析判断和实际应用,理解概念是解题关键,题目较简单.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
下列图示与对应的叙述相符的是( )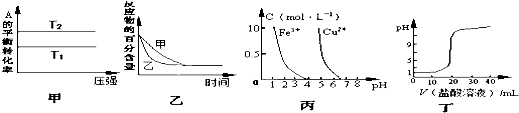

| A、由图甲可以判断:若T1>T2,反应A(g)+B(g)?2C(g)的△H>0 |
| B、图乙表示压强对可逆反应2A(g)+2B(g)?4C(g)+D(s)的影响,乙的压强比甲大 |
| C、根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 |
| D、图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,pH随加入盐酸体积的变化 |
下列金属中,通常采用还原法冶炼的是( )
| A、Na | B、Al | C、Fe | D、Ag |
根据热化学方程式:S(s)+O2(g)═SO2(g)△H=a kJ?mol-1(a=-297.2).分析下列说法,其中不正确的是( )
| A、S(s)在O2(g)中燃烧的反应是放热反应 |
| B、S(g)+O2(g)═SO2(g)△H=b kJ?mol-1,则a>b |
| C、1mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
| D、16g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量 |