题目内容
下列图示与对应的叙述相符的是( )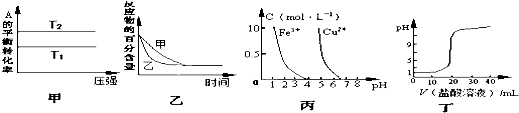

| A、由图甲可以判断:若T1>T2,反应A(g)+B(g)?2C(g)的△H>0 |
| B、图乙表示压强对可逆反应2A(g)+2B(g)?4C(g)+D(s)的影响,乙的压强比甲大 |
| C、根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 |
| D、图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,pH随加入盐酸体积的变化 |
考点:化学平衡的影响因素,化学平衡建立的过程,难溶电解质的溶解平衡及沉淀转化的本质,酸碱混合时的定性判断及有关ph的计算
专题:图示题
分析:A、升高温度A的转化率减小,平衡逆向移动,正反应是放热反应;
B、对于2A(g)+2B(g)?4C(g)+D(s)的反应,乙先拐说明乙的压强比甲大;
C、若除去CuSO4溶液中的Fe3+,根据图丙,可向溶液中加入适量NaOH溶液,调节pH4到5,使铁离子完全沉淀,而铜离子不能沉淀;
D、用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,未滴入盐酸时开始pH为13.
B、对于2A(g)+2B(g)?4C(g)+D(s)的反应,乙先拐说明乙的压强比甲大;
C、若除去CuSO4溶液中的Fe3+,根据图丙,可向溶液中加入适量NaOH溶液,调节pH4到5,使铁离子完全沉淀,而铜离子不能沉淀;
D、用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,未滴入盐酸时开始pH为13.
解答:
解:A、升高温度A的转化率减小,平衡逆向移动,正反应是放热反应,所以△H<0,故A错误;
B、对于2A(g)+2B(g)?4C(g)+D(s)的反应,乙先拐说明乙的压强比甲大,两边的气体的计量数相等,所以压强改变只改变速度,平衡不移动,故B正确;
C、若除去CuSO4溶液中的Fe3+,根据图丙,可向溶液中加入适量NaOH溶液,调节pH4到5,使铁离子完全沉淀,而铜离子不能沉淀,加适量NaOH溶液,引入钠离子,故C错误;
D、用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,未滴入盐酸时开始pH为13,故D错误;
故选B.
B、对于2A(g)+2B(g)?4C(g)+D(s)的反应,乙先拐说明乙的压强比甲大,两边的气体的计量数相等,所以压强改变只改变速度,平衡不移动,故B正确;
C、若除去CuSO4溶液中的Fe3+,根据图丙,可向溶液中加入适量NaOH溶液,调节pH4到5,使铁离子完全沉淀,而铜离子不能沉淀,加适量NaOH溶液,引入钠离子,故C错误;
D、用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,未滴入盐酸时开始pH为13,故D错误;
故选B.
点评:本题考查了除杂的试剂的选择,平衡的移动和电解质的相关知识,依据除杂的原则分析,注意三价铁离子的去除,常通过对Fe3+水解平衡的影响角度解答.

练习册系列答案
相关题目
下列现象或事实可用同一原理解释的是( )
| A、铁分别加入浓硫酸和氢氧化钠溶液中均无明显现象 |
| B、SO2既能使品红褪色也能使酸性高锰酸钾褪色 |
| C、漂白粉溶液和硅酸钠溶液久置空中都变质 |
| D、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率 |
水的三态的熵值的大小关系正确的是(Sm表示1mol物质的熵值)( )
| A、Sm(s)>Sm(l)>Sm(g) |
| B、Sm(l)>Sm(s)>Sm(g) |
| C、Sm(g)>Sm(l)>Sm(s) |
| D、Sm(s)=Sm(l)=Sm(g) |
25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
| A、C(s)+12O2(g)=CO(g)△H=-393.5 kJ/mol |
| B、2H2(g)+O2(g)=2H2O(l)△H=+571.6 kJ/mol |
| C、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ/mol |
| D、C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H=-2800 kJ/mol |
224mL某气体在标准状况下的质量为0.32g,该气体的摩尔质量为( )
| A、32g?mol-1 |
| B、64 |
| C、64g?mol-1 |
| D、64g |