��Ŀ����
14��X��Y��Z��R�����ֶ���������Ԫ�أ�Xԭ�������������Ǵ�����2����YԪ���ڵؿ��к�����࣬Z Ԫ�ؽ�������ǿ��Rԭ�ӵĺ����������X��Z���������֮�ͣ���������һ����ȷ���ǣ�������| A�� | ����������R��X | B�� | ���⻯���ȶ���Y��X | ||
| C�� | ��������ϼ�Z��X��Y��R | D�� | ��Z��R�γɵĻ�����Ϊ���ӻ����� |
���� X��Y��Z��R�Ƕ���������Ԫ�أ�Xԭ�������������Ǵ�����2����ԭ��ֻ����2�����Ӳ㣬����������Ϊ4����XΪC��YԪ���ڵؿ��к�����࣬��YΪO��ZԪ�ؽ�������ǿ����ZΪNa��Rԭ�ӵĺ����������X��Z���������֮�ͣ�Rԭ�Ӻ��������Ϊ6+11=17����RΪCl��
��� �⣺X��Y��Z��R�Ƕ���������Ԫ�أ�Xԭ�������������Ǵ�����2����ԭ��ֻ����2�����Ӳ㣬����������Ϊ4����XΪC��YԪ���ڵؿ��к�����࣬��YΪO��ZԪ�ؽ�������ǿ����ZΪNa��Rԭ�ӵĺ����������X��Z���������֮�ͣ�Rԭ�Ӻ��������Ϊ6+11=17����RΪCl��
A��̼������Ա�HClO������ǿ����A����
B���ǽ���Y��O����X��C�������⻯���ȶ��ԣ�ˮ�����飬��B����
C����Ԫ��û����������ϼۣ���C����
D����Z��R�γɵĻ�����Ϊ�����ơ��������ƣ����������ӻ������D��ȷ��
��ѡ��D��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã�ע���Ԫ����������Ԫ�ػ�����ṹ���ʵ����գ�Aѡ��ѧ����������ۺ����������жϣ�

��ϰ��ϵ�д�
�����Ŀ
5�������£�ij��Ӧ�ﵽƽ�⣬ƽ�ⳣ��K=$\frac{[CO][{H}_{2}O]}{[C{O}_{2}][{H}_{2}]}$�����������������䣬���¶����ߣ�c��H2����С���Ը÷�Ӧ�ķ�����ȷ���ǣ�������
| A�� | ��Ӧ�Ļ�ѧ����ʽΪ��CO+H2O?CO2+H2 | |
| B�� | �����¶ȣ�v��������v���棩��������v���棩������� | |
| C�� | ��С���������v��������v���棩��������v������������� | |
| D�� | �����¶Ȼ���С�����������������ƽ����Է����������ᷢ���ı� |
2������˵������ȷ���ǣ�������
| A�� | �����Խ����и������������ⸯʴ������pH���߷���������ʴ�ļ������� | |
| B�� | ���ˮ����ȹ����ԭˮ��������ܻ����������� | |
| C�� | �������ڳ��ٽ�CO2���к�ǿ���ܽ��ԣ���ȡ������ʱ���ó��ٽ�CO2����ȡ�� | |
| D�� | �ƻ������NOx�Ĵ�ת�����ǽ��������Ⱦ����Ĵ�ʩ |
6������˵������ȷ���ǣ�������
| A�� | ����������еĵ�������������ú������⻯ѧ�����������彡����ֲ��ɳ��ȶ��кܴ�Σ�� | |
| B�� | ũҵ����������빤ҵ�л������P�������ж��̲��ŷḻ���������� | |
| C�� | �ֹ��ȼƿ����ڷ�����Һ��ɫ�뷴Ӧ����������ĸ���Ũ�ȵĹ�ϵ���Ӷ�ȷ����ѧ��Ӧ���� | |
| D�� | ijЩ���������γɵķ���ɸ����������״��Ѩ��ͨ���������ڷ��롢�ᴿ�����Һ���������������������ӽ���������������������� |
3���л���X�ķ�����ΪC6H10O2����ϡ�����м��ȿɵõ�Y��Z�������ʣ�����Y��ʹ���CCl4��Һ��ɫ������NaHCO3��Һ��Ӧ�ҷ�����ֻ����һ��������X����У������������칹����������
| A�� | 7�� | B�� | 6�� | C�� | 5�� | D�� | 4�� |
10��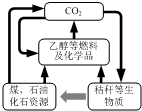 �ҹ�����������Դ��������̼��Դ�ĸ�Чת����ѭ�����ã���ͼ��ʾ������������������������Υ�����ǣ�������
�ҹ�����������Դ��������̼��Դ�ĸ�Чת����ѭ�����ã���ͼ��ʾ������������������������Υ�����ǣ�������
 �ҹ�����������Դ��������̼��Դ�ĸ�Чת����ѭ�����ã���ͼ��ʾ������������������������Υ�����ǣ�������
�ҹ�����������Դ��������̼��Դ�ĸ�Чת����ѭ�����ã���ͼ��ʾ������������������������Υ�����ǣ�������| A�� | ������չú��������Һ������ | B�� | �ӿ�ʯ�͵Ȼ�ʯȼ�ϵĿ��ɺ�ʹ�� | ||
| C�� | ��CO2 Ϊԭ�������ɽ������� | D�� | ���ոѽ��мӹ�ת��Ϊ�Ҵ�ȼ�� |
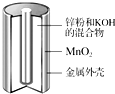 ����п�̸ɵ����������Ӧ�����ձ�ĵ��֮һ����ṹ��ͼ��ʾ����֪��طŵ��IJ�����Zn��OH��2��MnOOH��
����п�̸ɵ����������Ӧ�����ձ�ĵ��֮һ����ṹ��ͼ��ʾ����֪��طŵ��IJ�����Zn��OH��2��MnOOH�� ��
��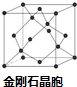 A��B��C��D��EΪԭ�������������������Ԫ�أ�A��һ��ͬλ�ؿ����ڿ����вⶨ�������������� B��Aͬ���ڣ���s�ܼ���������p�ܼ��������ࣻCԭ�ӵ������������Ǵ�����3����D��Bͬ���壻E��ԭ������Ϊ29���ش��������⣺
A��B��C��D��EΪԭ�������������������Ԫ�أ�A��һ��ͬλ�ؿ����ڿ����вⶨ�������������� B��Aͬ���ڣ���s�ܼ���������p�ܼ��������ࣻCԭ�ӵ������������Ǵ�����3����D��Bͬ���壻E��ԭ������Ϊ29���ش��������⣺ ��
��