题目内容
18.氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)步骤1:用碳酸钠溶液洗去铁屑表面的油污.
步骤2:加入稍过量的稀硫酸,保持50~80℃,充分反应后,过滤.
步骤3:将滤液与稍过量的NH4HCO3溶液混合,得到FeCO3的浊液.
步骤4:过滤、洗涤、干燥,得到FeCO3固体.
步骤5:煅烧FeCO3,得到Fe2O3固体.
(1)步骤2中,如何判断反应已经充分?溶液中不再产生气泡.
(2)步骤2所得的滤渣中主要含有一种铁的化合物W(Fe3C),经以下处理后,回收利用:W在足量的空气中高温煅烧,生成有磁性的固体X;将X溶于稀硫酸.
①煅烧时1mol W消耗O23mol;
②X溶于稀硫酸的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
(3)步骤3生成FeCO3反应的化学方程式为FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O.
(4)将步骤4补充完整:过滤、洗涤.
(5)若煅烧时条件控制不当,会使产品中存在杂质FeO.
①若要设计实验检验产品中是否存在FeO,且只能选用两种试剂,这两种试剂是稀硫酸和酸性KMnO4溶液.
②现煅烧116.0kg的FeCO3,得到79.2kg产品,则该产品的纯度为90.9%.(设产品中只有一种杂质FeO,计算结果保留3位有效数字)
分析 由步骤可知,碳酸钠水解显碱性,可促进油污的水解,加稀硫酸除去碳酸钠,且溶解Fe,过滤后,滤液中含Fe2+,与碳酸氢铵反应生成碳酸亚铁沉淀,经过过滤,洗涤,干燥,灼烧得到氧化铁;
(1)根据反应已经充分时反应停止即无现象发生判断;
(2)①Fe3C在足量的空气中高温煅烧,生成有磁性的固体X,X为Fe3O4,所以该反应方程式为:Fe3C+3O2$\frac{\underline{\;高温\;}}{\;}$Fe3O4+CO2,据此计算;
②X为Fe3O4,将X溶于稀硫酸反应生成硫酸亚铁、硫酸铁,据此书写离子方程式;
(3)步骤2滤液中含Fe2+,与碳酸氢铵反应生成碳酸亚铁沉淀,据此书写离子方程式;
(4)将步骤4经过过滤,洗涤,干燥,得到FeCO3固体;
(5)①根据以上分析煅烧后肯定生成氧化铁,要检验产品中是否存在FeO,则应先用酸将其溶解,再用酸性KMnO4溶液检验含有三价铁离子时是否含有二价铁离子;
②假设Fe2O3物质的量为x mol,FeO的物质的量为y mol,根据质量守恒和铁原子守恒列方程组计算.
解答 解:(1)因为反应已经充分时反应停止即无现象发生,所以当溶液中不再产生气泡时可以判断反应已经充分,
故答案为:溶液中不再产生气泡;
(2)①Fe3C在足量的空气中高温煅烧,生成有磁性的固体X,X为Fe3O4,所以该反应方程式为:Fe3C+3O2$\frac{\underline{\;高温\;}}{\;}$Fe3O4+CO2,则煅烧时1mol W(Fe3C),消耗O2 3mol,
故答案为:3;
②X为Fe3O4,将X溶于稀硫酸反应生成硫酸亚铁、硫酸铁,则离子方程式为 Fe3O4+8H+=2Fe3++Fe2++4H2O,
故答案为:Fe3O4+8H+=2Fe3++Fe2++4H2O;
(3)步骤2滤液中含Fe2+,与碳酸氢铵反应生成碳酸亚铁沉淀,则生成FeCO3沉淀的化学方程式为FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O,故答案为:FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O;
(4)将步骤4经过过滤,洗涤,干燥,得到FeCO3固体,故答案为:过滤;洗涤;
(5)①根据以上分析煅烧后肯定生成氧化铁,要检验产品中是否存在FeO,则应先用酸将其溶解,再用酸性KMnO4溶液检验含有三价铁离子时是否含有二价铁离子,又酸性KMnO4溶液会氧化氯离子,所以应选用硫酸溶解,所以这两种试剂是稀硫酸和酸性KMnO4溶液,
故答案为:稀硫酸和酸性KMnO4溶液;
②假设Fe2O3物质的量为x mol,FeO的物质的量为y mol,那么满足:160x+72y=79200;铁原子守恒(2x+y)×116=116000,解得x=450mol,所以产物中Fe2O3的质量160g/mol×450mol=72000g=72kg,则该产品的纯度为$\frac{72g}{79.2g}$×100%=90.9%;故答案为:90.9%.
点评 本题考查元素化合物性质、基本操作与方案设计、常用化学用语等,关键是熟练综合应用相关元素化合物知识,要求学生要有扎实的实验基础知识和灵活应用信息解决问题的能力,题目难度中等.

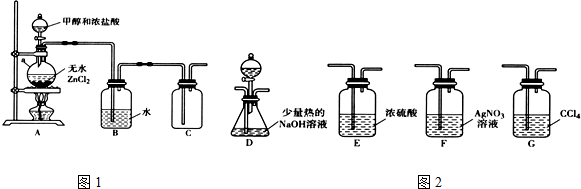
①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为CH3OH+HCl$→_{△}^{ZnCl_{2}}$CH3Cl+H2O.
②装置B的主要作用是除去氯化氢气体.
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L-1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L-1盐酸标准液对吸收液进行返滴定(发生的反应为:
NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+2CO2↑+2H2O),最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为(c1V1-c2V2)×10-3 _ mol.(已知:2CH3Cl+3O2$\stackrel{点燃}{→}$2CO2+2H2O+2HCl)
(2)乙组同学选用甲组A、B装置和图2所示的部分装置检验CH3Cl中的氯元素.
(已知:一卤代烷一般要在加热条件下才能与氢氧化钠溶液反应)
①乙组同学的实验装置中,依次连接的合理顺序为A→B→F→D→G.
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞,观察实验现象.分液漏斗中盛放的试剂是硝酸和硝酸银溶液.
③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成.
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子.相关数据如表:
| 化学键 | C-Cl | C-Br |
| 键能(kJ•mol-1) | 330 | 276 |
| 化合物 | AgCl | AgBr |
| Ksp近似值 | 1.8×10-10 | 5×10-13 |
③将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀.请依据表中数据解释原因C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀.
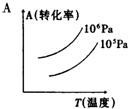 有一化学平衡mA(g)+nB(g)═PC(g)+qD(g),如图表示的转化率与压强、温度的关系.由此得出的正确结论是( )
有一化学平衡mA(g)+nB(g)═PC(g)+qD(g),如图表示的转化率与压强、温度的关系.由此得出的正确结论是( )| A. | 正反应是吸热反应,(m+n)>(p+q) | B. | 正反应是吸热反应,(m+n)<(p+q) | ||
| C. | 正反应是放热反应,(m+n)>(p+q) | D. | 正反应是放热反应,(m+n)<(p+q) |
| A. | 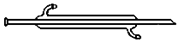 | B. | 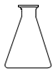 | ||
| C. | 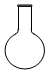 | D. | 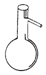 |
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| C. | 锌片插入硝酸银溶液中:Zn+Ag+═Zn2++Ag | |
| D. | 硫酸溶液与氢氧化铜反应:H++OH-═H2O |
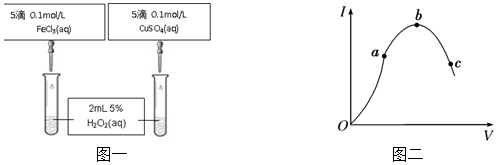
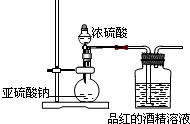
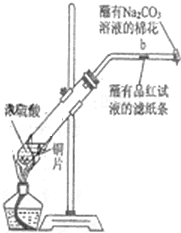 如图所示,将6.4g铜与12mL18mol•L-1浓硫酸在试管a中共热.据此回答:
如图所示,将6.4g铜与12mL18mol•L-1浓硫酸在试管a中共热.据此回答: