题目内容
14.下列关于芳香族化合物 说法正确的是( )
说法正确的是( )| A. | 1 molA能与4 mol Ag(NH3)2OH溶液发生银镜反应 | |
| B. | 核磁共振氢谱图显示有三个吸收峰 | |
| C. | 不能与FeCl3溶液发生显色反应 | |
| D. | 1 mol A能与2 mol NaHCO3完全反应放出CO2 |
分析 该物质中含有醛基、酚羟基和苯环,具有醛、酚和苯的性质,能发生氧化反应、还原反应、加成反应、取代反应、显色反应等,据此分析解答.
解答 解:A.该分子中含有两个醛基,所以1 molA能与4 mol Ag(NH3)2OH溶液发生银镜反应,故A正确;
B.该分子中含有4种氢原子,所以核磁共振氢谱有4个吸收峰,故B错误;
C.含有酚羟基,所以能与氯化铁溶液发生显色反应,故C错误;
D.不含羧基,所以不能和碳酸氢钠反应,故D错误;
故选A.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,侧重考查酚、醛的性质,注意酚羟基和碳酸钠反应但和碳酸氢钠不反应,为易错点.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
5.下列说法正确的是( )
| A. | 利用新制氢氧化铜悬浊液可以鉴别有机物中是否含醛基 | |
| B. | 所有的醇都可以发生消去反应生成烯烃 | |
| C. | 羧酸不一定可以与碳酸钠溶液反应 | |
| D. | 苯酚的酸性很弱,不能使指示剂变色,但可以和碳酸氢钠溶液反应放出CO2 |
2.用CH4催化还原NO,可以消除氮氧化物的污,有望解决汽车尾气污染问题,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-akJ•mol-1
按上述转化,标准状况下44.8L NO2被还原至N2,整个过程中放出的热量为867kJ,则a的值为( )
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-akJ•mol-1
按上述转化,标准状况下44.8L NO2被还原至N2,整个过程中放出的热量为867kJ,则a的值为( )
| A. | 1160 | B. | 2308 | C. | 1441 | D. | 2320 |
19.通过复习总结,下列归纳正确的是( )
| A. | 有单质参加的反应,置换反应一定都属于氧化还原反应 | |
| B. | 简单非金属阴离子只有还原性,而金属阳离子只有氧化性 | |
| C. | 离子化合物在熔融态都能够导电,共价化合物在熔融态都不导电 | |
| D. | 所有物质都有化学键 |
3.禁止用工业酒精配制饮用酒,这是因为酒精中含有的少量有毒物质是( )
| A. | 甘油 | B. | 醋酸 | C. | 甲醇 | D. | 乙醛 |
4.图表法、图象法是常用的科学研究方法.请回答以下问题
(1)第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
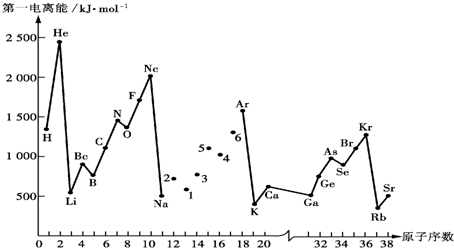
①将Na-Ar之间六种元素用短线连接起来(不必写在答题卷上),构成完整的图象.从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次减小
②上图折线中数字5代表元素在周期表中的位置是第三周期ⅤA族;
(2)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:试结合元素周期律知识完成下列问题:
①经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键(填离子键或共价键).
②某有机化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(3)已知:波长为300nm的紫外光的光子所具有的能量约为399kJ/mol.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
(1)第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图.

①将Na-Ar之间六种元素用短线连接起来(不必写在答题卷上),构成完整的图象.从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次减小
②上图折线中数字5代表元素在周期表中的位置是第三周期ⅤA族;
(2)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:试结合元素周期律知识完成下列问题:
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
②某有机化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(3)已知:波长为300nm的紫外光的光子所具有的能量约为399kJ/mol.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
| C--C | C--N | C--S | |
| 键能 KJ/mol | 347 | 305 | 259 |
