题目内容
5.下列说法正确的是( )| A. | 利用新制氢氧化铜悬浊液可以鉴别有机物中是否含醛基 | |
| B. | 所有的醇都可以发生消去反应生成烯烃 | |
| C. | 羧酸不一定可以与碳酸钠溶液反应 | |
| D. | 苯酚的酸性很弱,不能使指示剂变色,但可以和碳酸氢钠溶液反应放出CO2 |
分析 A.醛基具有还原性,可与弱氧化剂发生氧化还原反应;
B.只有羟基邻位碳原子含有氢原子时才能发生消去反应;
C.羧酸酸性比碳酸强;
D.苯酚的酸性比碳酸弱.
解答 解:A.醛基具有还原性,可与氢氧化铜浊液在加热条件下发生氧化还原反应,可用于检验醛基,故A正确;
B.只有羟基邻位碳原子含有氢原子时才能发生消去反应,故B错误;
C.羧酸酸性比碳酸强,可与碳酸钠反应,故C错误;
D.苯酚的酸性比碳酸弱,与碳酸氢钠溶液不反应,故D错误.
故选A.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握常见机物的结构和官能团的性质,难度不大.

练习册系列答案
相关题目
2.某学习小组探究金属与不同酸反应的差异,以及影响反应速率的因素.
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g.
(1)帮助该组同学完成以上实验设计表.
(2)该小组同学在对比①和⑤实验时发现①的反应速度都明显比⑤快,你能对问题原因作出哪些假设或猜想(列出一种即可)?Cl-能够促进Al与H+的反应或SO42-对Al与H+的反应起阻碍作用.
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g.
(1)帮助该组同学完成以上实验设计表.
| 实验目的 | 实验编号 | 温度 | 金属铝的形态 | 酸及浓度 |
| 1.实验①和②探究盐酸浓度对该反应速率的影响 2.实验②和③探究探究温度对反应速率的影响 3.实验②和④探究金属规格(铝片,铝粉)对该反应速率的影响 4.①和⑤实验探究铝与稀盐酸和稀硫酸反应的差异 | ① | 25℃ | 铝片 | 4.0moL/L盐酸 |
| ② | 25℃ | 铝片 | 2.0moL/L盐酸 | |
| ③ | 35℃ | 铝片 | 2.0moL/L盐酸 | |
| ④ | 25℃ | 铝粉 | 2.0moL/L盐酸 | |
| ⑤ | 25℃ | 铝片 | 2.0moL/L硫酸 |
16.某烃的一种同分异构体的一氯代物只有一种,该烃的分子式是( )
| A. | C6H14 | B. | C5H12 | C. | C4H10 | D. | C3H8 |
13.下列说法正确的是( )
| A. | 在常温常压下,11.2L N2含有的分子数为0.5NA | |
| B. | 32g O2含原子数目为2NA | |
| C. | 标准状况下,18g H2O所占的体积为22.4L | |
| D. | 在同温同压下,相同体积任何气体单质所含的原子数目相同 |
10.下列化合物中,既显酸性,又能发生加成反应、氧化反应、酯化反应和消去反应的是( )
| A. | 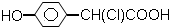 | B. | CH3CH (OH)-CH=CH-COOH | ||
| C. | CH3-CH=CH-COOH | D. | CH3CH(OH)CH2CHO |
14.下列关于芳香族化合物 说法正确的是( )
说法正确的是( )
 说法正确的是( )
说法正确的是( )| A. | 1 molA能与4 mol Ag(NH3)2OH溶液发生银镜反应 | |
| B. | 核磁共振氢谱图显示有三个吸收峰 | |
| C. | 不能与FeCl3溶液发生显色反应 | |
| D. | 1 mol A能与2 mol NaHCO3完全反应放出CO2 |

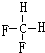 和
和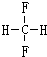
 和CH2=CH-CH2
和CH2=CH-CH2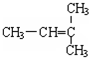 和
和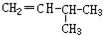
 .
.