题目内容
4.化学与生产、生活息息相关,下列有关说法正确的是( )| A. | 树林晨曦中见到的缕缕阳光,是丁达尔效应效应造成的 | |
| B. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| C. | 神舟11号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是二氧化硅 | |
| D. | 尽量使用含12C的产品,减少使用含13C或14C的产品符合“促进低碳经济”宗旨 |
分析 A.丁达尔现象为胶体特有的性质;
B.汽油的主要成分是含碳原子5~11个的烃,烃为碳氢化合物,高温富氧环境造成氮的氧化物,与汽油不完全燃烧无关;
C.Si为半导体材料;
D.12C、13C或14C的产品均燃烧生成二氧化碳.
解答 解:A.丁达尔现象为胶体特有的性质,则树林晨曦中见到的缕缕阳光,是丁达尔效应效应造成的,故A正确;
B.机动车在行驶中烃类不完全燃烧,产生一氧化碳甚至冒黑烟,汽车尾气排放的氮氧化物是在汽车发动机气缸内高温富氧环境下氮气和氧气的反应,不是汽油不完全燃烧造成的,故B错误;
C.神舟11号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是硅,二氧化硅为光纤的材料,故C错误;
D.12C、13C或14C的产品均燃烧生成二氧化碳,均应减少使用,促进低碳经济,故D错误;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、环境保护、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
15.下列物质的沸点按由高到低顺序排列正确的是( )
①丙三醇
②丁烷
③乙二醇
④乙醇.
①丙三醇
②丁烷
③乙二醇
④乙醇.
| A. | ①②③④ | B. | ④③②① | C. | ②①③④ | D. | ①③④② |
12.下列实验操作能达到目的是( )
| 实验目的 | 实验操作 | |
| A | 区分苯和四氯化碳 | 在两支分别盛有少量苯和四氯化碳的试管中加碘水后振荡 |
| B | 证明溴乙烷中有溴原子 | 溴乙烷与NaOH水溶液共热,充分反应,冷却后加入硝酸银溶液 |
| C | 制取溴苯 | 在苯中加铁粉后再加溴水并振荡 |
| D | 除去苯中的甲苯 | 向混合物中加入酸性高锰酸钾溶液,然后分液 |
| A. | A | B. | B | C. | C | D. | D |
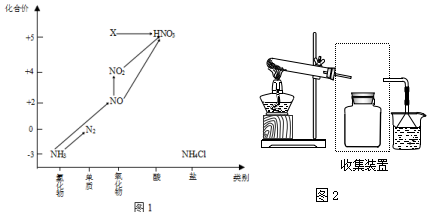
9.利用图1和图2中的信息,按图3装置(连接的A、B瓶中已充有NO2气体)进行实验.

下列说法正确的是( )

下列说法正确的是( )
| A. | H2O2中只含有极性共价键,不含离子键 | |
| B. | 2NO2?N2O4的平衡常数K随温度升高而减小 | |
| C. | 向H2O2中加入Fe2(SO4)3后,B中颜色变浅 | |
| D. | H2O2分解反应中Fe2(SO4)3作催化剂,可以使反应的△H减小 |
16.按要求填写下列空白:
(1)将10molA 和smolB 充入SL 密闭容器中,某温度下发生反应:3A+B?2C ( A、B、C均为气体),在最初2s内,v(A)为0.6mol/(L•s).则在2s时,B的物质的量浓度为0.6mol/L,C 的体积分数为$\frac{0.8S}{10-S}$×100%(小数点后保留一位).
(2)某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL1.0mol/L盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况),实验记录如表(累计值)
①哪一时间段(0-1min、1-2min、2-3min、3-4min、4-5min)反应速率最慢4~5min,原因是因为4~5min时H+浓度小(或酸的浓度小).
②求2-3min时间段内以盐酸的浓度变化表示的该反应的反应速率0.1mol/(L•min)(忽略溶液体积的变化).
③为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列}溶液:
A.蒸馏水 B.NaCl溶液 C.0.5mol/L盐酸
你认为可行的是(填序号)ABC.
(1)将10molA 和smolB 充入SL 密闭容器中,某温度下发生反应:3A+B?2C ( A、B、C均为气体),在最初2s内,v(A)为0.6mol/(L•s).则在2s时,B的物质的量浓度为0.6mol/L,C 的体积分数为$\frac{0.8S}{10-S}$×100%(小数点后保留一位).
(2)某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL1.0mol/L盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况),实验记录如表(累计值)
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
②求2-3min时间段内以盐酸的浓度变化表示的该反应的反应速率0.1mol/(L•min)(忽略溶液体积的变化).
③为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列}溶液:
A.蒸馏水 B.NaCl溶液 C.0.5mol/L盐酸
你认为可行的是(填序号)ABC.
13.阿托酸甲酯(Y)能用于治疗肠道疾病,它可由阿托酸(X)经过下列反应合成:

下列说法正确的是( )

下列说法正确的是( )
| A. | X可用于合成高分子化合物,Y不能合成高分子化合物 | |
| B. | X在烧碱溶液中变质,而Y在烧碱溶液中不变质 | |
| C. | X分子中所有原子均可能共平面 | |
| D. | X和Y分别与浓硝酸反应都能生成5种二硝基取代物 |