题目内容
12.下列实验操作能达到目的是( )| 实验目的 | 实验操作 | |
| A | 区分苯和四氯化碳 | 在两支分别盛有少量苯和四氯化碳的试管中加碘水后振荡 |
| B | 证明溴乙烷中有溴原子 | 溴乙烷与NaOH水溶液共热,充分反应,冷却后加入硝酸银溶液 |
| C | 制取溴苯 | 在苯中加铁粉后再加溴水并振荡 |
| D | 除去苯中的甲苯 | 向混合物中加入酸性高锰酸钾溶液,然后分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.苯的密度与水的密度小,四氯化碳的密度比水的密度大;
B.水解后加酸至酸性,再检验;
C.苯与溴水不反应;
D.甲苯被氧化后,与苯分层.
解答 解:A.与碘水混合后,分层现象不同,可鉴别,故A正确;
B.水解后加酸至酸性,再检验,则没有加硝酸至酸性,不能检验,故B错误;
C.应苯、液溴、铁粉制备溴苯,故C错误;
D.甲苯被氧化后,与苯分层,然后分液可分离,故D正确;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2. 氢是一种清洁的可再生能源.
氢是一种清洁的可再生能源.
(1)已知:
若1g水蒸气变为液态水时放出2.4KJ热量,则表示氢气燃烧热的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.2kJ/mol.
(2)氢的稳定存储是氢能源发展的关键.固态合金具有较强的吸附氢原子能力,其原理可表示为(以M代表固态合金):2M(s)+xH2(g) $?_{释放}^{存储}$2MHx(s)△H<0
①有利于氢气存储的条件为低温,高压;
②该反应的平衡常数的表达式为$K=\frac{1}{{{c^x}({H_2})}}$;
③达平衡后保持恒温恒压下增加氢气的量,该平衡向右移动(填“向左”、“向右”、或“不”)
(3)储氢合金可做二次电池的电极,其工作原理为:xNi(OH)2+M$?_{放电}^{充电}$MHx+xNiOOH.装置如图所示:
①a为电源的负极;
②写出充电时阴极反应式xH2O+xe-+M=MHx+xOH-;
③以该电池做电源电解饱和NaCl溶液,当手机到标准状况下11.2LH2时,储氢合金理论上释放出1g氢,此时有1molOH-由B向A(填“A”或“B”)移动.
 氢是一种清洁的可再生能源.
氢是一种清洁的可再生能源.(1)已知:
| 化学键 | H-H(g) | H-O(g) | O≡O(g) |
| 键能(KJ/mol) | 436 | 463 | 496 |
(2)氢的稳定存储是氢能源发展的关键.固态合金具有较强的吸附氢原子能力,其原理可表示为(以M代表固态合金):2M(s)+xH2(g) $?_{释放}^{存储}$2MHx(s)△H<0
①有利于氢气存储的条件为低温,高压;
②该反应的平衡常数的表达式为$K=\frac{1}{{{c^x}({H_2})}}$;
③达平衡后保持恒温恒压下增加氢气的量,该平衡向右移动(填“向左”、“向右”、或“不”)
(3)储氢合金可做二次电池的电极,其工作原理为:xNi(OH)2+M$?_{放电}^{充电}$MHx+xNiOOH.装置如图所示:
①a为电源的负极;
②写出充电时阴极反应式xH2O+xe-+M=MHx+xOH-;
③以该电池做电源电解饱和NaCl溶液,当手机到标准状况下11.2LH2时,储氢合金理论上释放出1g氢,此时有1molOH-由B向A(填“A”或“B”)移动.
7.已知aXm+和bYn-两种离子的电子层结构相同,则b等于( )
| A. | a+m+n | B. | a+m-n | C. | a-m+n | D. | a-m-n |
17.下列说法中不正确的是( )
| A. | 碱金属元素锂、钠、钾、铷、铯,随着核电荷数的增加其单质的熔沸点逐渐降低 | |
| B. | 卤族元素氟、氯、溴、碘,随着核电荷数的增加其单质的熔沸点逐渐升高 | |
| C. | NaOH、KOH、Mg(OH)2的碱性依次减弱 | |
| D. | 在周期表中金属与非金属的分界处可以找到半导体材料 |
4.化学与生产、生活息息相关,下列有关说法正确的是( )
| A. | 树林晨曦中见到的缕缕阳光,是丁达尔效应效应造成的 | |
| B. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| C. | 神舟11号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是二氧化硅 | |
| D. | 尽量使用含12C的产品,减少使用含13C或14C的产品符合“促进低碳经济”宗旨 |
1.下列有关化学用语表示正确的是( )
| A. | 次氯酸的结构式:H-Cl-O | B. | 1H、2H、3H是同一种核素 | ||
| C. | S2-的结构示意图: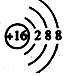 | D. | 四氯化碳的电子式: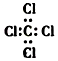 |
2.某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件.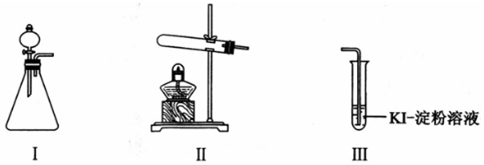
供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如表:
(2)丙实验中O2与KI溶液反应的离子方程式是O2+4I-+4H+=2I2+2H2O.
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是酸性环境.为进一步探究该条件对反应速率的影响,可采取的实验措施是使用不同浓度的稀硫酸作对比实验.
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝.学生将I中产生的气体直接通入下列AD溶液(填序号),证明了白雾中含有H2O2.
A.酸性 KMnO4 B.FeCl2 C.Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH.该小组同学取20mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)3I2+6OH-=5I-+IO3-+3H2O造成的,请设计实验证明他们的猜想是否正确在上述未变蓝的溶液中滴入0.1mol/LH2SO4溶液观察现象,若溶液变蓝则猜想正确,否则错误.

供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如表:
| 操作 | 现象 | |
| 甲 | 向I的锥形瓶中加入MnO2固体,.向I的分液漏斗中加入30% H2O2溶液,连接I、Ⅲ,打开活塞 | I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
| 乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
| 丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是酸性环境.为进一步探究该条件对反应速率的影响,可采取的实验措施是使用不同浓度的稀硫酸作对比实验.
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝.学生将I中产生的气体直接通入下列AD溶液(填序号),证明了白雾中含有H2O2.
A.酸性 KMnO4 B.FeCl2 C.Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH.该小组同学取20mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)3I2+6OH-=5I-+IO3-+3H2O造成的,请设计实验证明他们的猜想是否正确在上述未变蓝的溶液中滴入0.1mol/LH2SO4溶液观察现象,若溶液变蓝则猜想正确,否则错误.
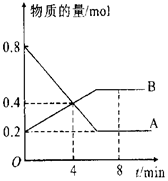 在一定条件下,在4L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,据图分析回答下列问题:
在一定条件下,在4L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,据图分析回答下列问题: