题目内容
不能确定为磷元素的化学用语是( )
| A、3s23p3 |
| B、(n+1)sn(n+1)pn+1 |
C、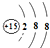 |
D、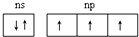 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:A、该微粒的核外电子排布式为[Ne]3s23p3,核外电子数为15,质子数为15;
B、s能级只有1个原子轨道,最多容纳2个电子,因此n=2,(n+1)sn(n+1)pn+1为3s23p3,与A选项相同;C、该微粒质子数为15,为磷元素;
D、不能确定粒子所处的能层,因此无法判断是否为磷元素.
B、s能级只有1个原子轨道,最多容纳2个电子,因此n=2,(n+1)sn(n+1)pn+1为3s23p3,与A选项相同;C、该微粒质子数为15,为磷元素;
D、不能确定粒子所处的能层,因此无法判断是否为磷元素.
解答:
解:A、该微粒的核外电子排布式为[Ne]3s23p3,核外电子数为15,质子数为15,是磷元素,故A不选;
B、s能级只有1个原子轨道,最多容纳2个电子,因此n=2,(n+1)sn(n+1)pn+1为3s23p3,与A选项相同,故B不选;
C、该微粒质子数为15,为磷元素,故C不选;
D、不能确定粒子所处的能层n,因此无法判断是否为磷元素,故D选;
故选D.
B、s能级只有1个原子轨道,最多容纳2个电子,因此n=2,(n+1)sn(n+1)pn+1为3s23p3,与A选项相同,故B不选;
C、该微粒质子数为15,为磷元素,故C不选;
D、不能确定粒子所处的能层n,因此无法判断是否为磷元素,故D选;
故选D.
点评:本题考查了化学语言代表的意义,掌握核外电子排布规律是解题的关键,难度一般,注意基础知识的积累.

练习册系列答案
相关题目
为了区别五瓶无色溶液:HCl、AlCl3、Ba(NO3)2,NaCl、Na2CO3,四位同学都没用酒精灯,三位同学另用了试剂,一位同学没有另用任何试剂.其中操作步骤一定最少的是( )
| A、甲另用了酚酞试液 |
| B、乙另用了NaOH溶液 |
| C、丙另用了石蕊试液 |
| D、丁不另用任何试剂 |
原子序数为26的Fe核外未成对的电子数为( )
| A、5 | B、4 | C、3 | D、2 |
下列表达方式正确的是( )
A、基态碳原子的价电子排布图: |
| B、HClO的结构式:H-Cl-O |
| C、基态26Fe的价电子排布式:3d64s2 |
D、基态铜原子的价电子排布图: |
下列各物质中,所有原子都满足最外层8电子结构的是( )
| A、BeCl2 |
| B、PCl3 |
| C、NH3 |
| D、PCl5 |
下列能大量共存且溶液为无色透明的离子组是( )
| A、Al3+、Na+、HCO3-、Cl- |
| B、Fe3+、NO3-、Cl-、SO42- |
| C、Na+、H+、SO32-、NO3- |
| D、SiO32-、Na+、K+、CO32- |

