题目内容
已知:A+B→X+Y+H2O(未配平,反应条件略去)是中学中常见反应的化学方程式,请回答:
(1)若在加热条件下发生的上述反应用于实验室制取一种使红色石蕊试纸变蓝的气体,则该反应的化学方程式是 .
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,则A与B的反应中氧化剂与还原剂的物质的量之比是 .
(3)若A为金属单质,其对应的氢氧化物为无色,其与B的浓溶液常温钝化而加热则可以反应并产生红棕色的气体,则此反应的离子方程式为 ,所得的1mol气体充入水中,若保证被完全吸收,则同时应充入标准状态下氧气 L.
(4)若A为非金属固体单质,X、Y是两种无色气体,则该反应所得的还原产物化学式为 ,氧化产物的电子式为 ;反应的化学方程式是 .
(1)若在加热条件下发生的上述反应用于实验室制取一种使红色石蕊试纸变蓝的气体,则该反应的化学方程式是
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,则A与B的反应中氧化剂与还原剂的物质的量之比是
(3)若A为金属单质,其对应的氢氧化物为无色,其与B的浓溶液常温钝化而加热则可以反应并产生红棕色的气体,则此反应的离子方程式为
(4)若A为非金属固体单质,X、Y是两种无色气体,则该反应所得的还原产物化学式为
考点:无机物的推断
专题:推断题
分析:(1)若在加热条件下,发生的上述反应用于实验室制取一种使红色石蕊试纸变蓝的气体,则该气体为氨气,该反应为氯化铵与氢氧化钙反应制备氨气;
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,该反应是Fe与浓硫酸反应生成硫酸铁、二氧化硫与水;
(3)若A为金属单质,其对应的氢氧化物为无色,其与B的浓溶液常温钝化而加热则可以反应并产生红棕色的气体,则A为Al,B为浓硝酸,二者反应生成硝酸铝、二氧化氮与水;
(4)若A为非金属固体单质,X、Y是两种无色气体,则A为碳、B为浓硫酸,二者反应生成二氧化碳、二氧化硫与水,二氧化硫为还原产物,二氧化碳是氧化产物.
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,该反应是Fe与浓硫酸反应生成硫酸铁、二氧化硫与水;
(3)若A为金属单质,其对应的氢氧化物为无色,其与B的浓溶液常温钝化而加热则可以反应并产生红棕色的气体,则A为Al,B为浓硝酸,二者反应生成硝酸铝、二氧化氮与水;
(4)若A为非金属固体单质,X、Y是两种无色气体,则A为碳、B为浓硫酸,二者反应生成二氧化碳、二氧化硫与水,二氧化硫为还原产物,二氧化碳是氧化产物.
解答:
解:(1)若在加热条件下,发生的上述反应用于实验室制取一种使红色石蕊试纸变蓝的气体,则该气体为氨气,该反应为氯化铵与氢氧化钙反应制备氨气,反应方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,该反应是Fe与浓硫酸反应生成硫酸铁、二氧化硫与水,反应方程式为:2Fe+6H2SO4(浓)=Fe2(SO4)3+3SO2↑+6H2O,Fe为还原剂,硫酸起氧化剂、酸性作用,起氧化剂的硫酸生成二氧化硫,故反应中氧化剂与还原剂的物质的量之比是3:2,
故答案为:3:2;
(3)若A为金属单质,其对应的氢氧化物为无色,其与B的浓溶液常温钝化而加热则可以反应并产生红棕色的气体,则A为Al,B为浓硝酸,二者反应生成硝酸铝、二氧化氮与水,反应离子方程式为:Al+6H++3NO3-
Al3++3NO2↑+3H2O,1molNO2充入水中,若保证被完全吸收,由电子转移守恒需要氧气为
=0.25mol,故需要通入氧气为0.25mol×22.4L/mol=5.6L,
故答案为:Al+6H++3NO3-
Al3++3NO2↑+3H2O;5.6L;
(4)若A为非金属固体单质,X、Y是两种无色气体,则A为碳、B为浓硫酸,二者反应生成二氧化碳、二氧化硫与水,反应方程式为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,SO2为还原产物,CO2是氧化产物,其电子式为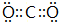 ,
,
故答案为:SO2;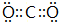 ;C+2H2SO4(浓)
;C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,该反应是Fe与浓硫酸反应生成硫酸铁、二氧化硫与水,反应方程式为:2Fe+6H2SO4(浓)=Fe2(SO4)3+3SO2↑+6H2O,Fe为还原剂,硫酸起氧化剂、酸性作用,起氧化剂的硫酸生成二氧化硫,故反应中氧化剂与还原剂的物质的量之比是3:2,
故答案为:3:2;
(3)若A为金属单质,其对应的氢氧化物为无色,其与B的浓溶液常温钝化而加热则可以反应并产生红棕色的气体,则A为Al,B为浓硝酸,二者反应生成硝酸铝、二氧化氮与水,反应离子方程式为:Al+6H++3NO3-
| ||
| 1mol |
| 4 |
故答案为:Al+6H++3NO3-
| ||
(4)若A为非金属固体单质,X、Y是两种无色气体,则A为碳、B为浓硫酸,二者反应生成二氧化碳、二氧化硫与水,反应方程式为:C+2H2SO4(浓)
| ||
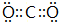 ,
,故答案为:SO2;
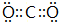 ;C+2H2SO4(浓)
;C+2H2SO4(浓)
| ||
点评:本题考查无机物推断,属于开放性题目,需要学生熟练掌握元素化合物知识,难度中等.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1 mol羟基(-OH)中含有的质子数为10 NA |
| B、相同状况下,22.4 L NO和11.2 L O2反应,生成物含有NA个分子 |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2 NA个电子 |
| D、1 mol Na2O2含有2 NA个阴离子 |
不能确定为磷元素的化学用语是( )
| A、3s23p3 |
| B、(n+1)sn(n+1)pn+1 |
C、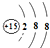 |
D、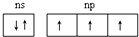 |
和氖原子有相同的电子层结构的微粒是( )
| A、He |
| B、K+ |
| C、Cl- |
D、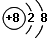 |
下列说法中不正确的是( )
| A、处于最低能量的原子叫做基态原子 |
| B、4f 4表示4f能级有四个轨道 |
| C、同一原子中,2p、3d、4f能级的轨道数依次增多 |
| D、同一原子中,2p、3p、4p电子的能量逐渐增大 |
下列有关电解质溶液中,说法正确的是( )
| A、0.2mol/L CH3COONa溶液和0.1mol/L HCl溶液等体积混合之后:c(Na+)=2c(Cl-)=c(CH3COO-)+c(CH3COOH)=0.2mol/L |
| B、0.1mol/LNa2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C、0.1mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| D、25℃时,向10mL pH=4的盐酸中,加入pH=10的一元碱BOH溶液至pH刚好等于7,则反应后的溶液总体积:V总≤20mL |
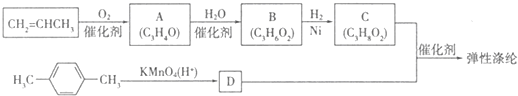
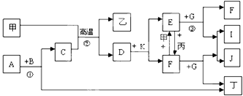 下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液.各物质间的转化如如图所示,回答下列各问题(部分生成物未列出):
下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液.各物质间的转化如如图所示,回答下列各问题(部分生成物未列出):