题目内容
某同学组装了如图所示的电化学装置,电极Ⅰ为Zn,其他电极均为Cu,则下列说法正确的是( )


| A、电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ |
| B、电极Ⅰ发生还原反应 |
| C、电极Ⅳ逐渐溶解 |
| D、电极Ⅲ的电极反应:Cu-2e-═Cu2+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电极Ⅰ为Zn,其它均为Cu,Zn易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,电子方向从负极流向正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,据此分析解答.
解答:
解:电极Ⅰ为Zn,其它均为Cu,Zn易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,
A.电子方向从负极流向正极,即电极Ⅰ→电极Ⅳ,电极Ⅲ→电极Ⅱ,电子不能通过溶液,故A错误;
B.电极Ⅰ上电极上为Zn失电子,发生氧化反应,故B错误;
C.电极Ⅳ是阴极,该电极上发生反应为Cu 2++2e-=Cu,所以电极质量逐渐增大,故C错误;
D.电极Ⅲ为阳极,电极反应式为Cu-2e-═Cu2+,故D正确;
故选D.
A.电子方向从负极流向正极,即电极Ⅰ→电极Ⅳ,电极Ⅲ→电极Ⅱ,电子不能通过溶液,故A错误;
B.电极Ⅰ上电极上为Zn失电子,发生氧化反应,故B错误;
C.电极Ⅳ是阴极,该电极上发生反应为Cu 2++2e-=Cu,所以电极质量逐渐增大,故C错误;
D.电极Ⅲ为阳极,电极反应式为Cu-2e-═Cu2+,故D正确;
故选D.
点评:本题考查了原电池原理,正确判断正负极是解本题关键,再结合各个电极上发生的反应来分析解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列可逆反应达平衡状态后,降温可以使混和气体平均相对分子质量减小的是( )
| A、H2(气)+Br2(气)?2HBr(气) (正反应为放热反应) |
| B、N2(气)+3H2(气)?2NH3(气) (正反应为放热反应) |
| C、2SO3(气)?2SO2(气)+O2(气) (正反应为吸热反应) |
| D、4NH3(气)+5O2(气)?4NO(气)+6H2O(气) (正反应为放热反应) |
以下现象与电化学腐蚀无关的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、生铁比纯铁容易生锈 |
| C、铁质器件附有铜质配件,在接触处易生铁锈 |
| D、银质物品久置表面变暗 |
下列反应与相应说法不正确的是( )
| A、SiO2+2NaOH═Na2SiO3+H2O说明SiO2是酸性氧化物 | ||||
B、SiO2+2C
| ||||
C、SiO2+Na2CO3
| ||||
| D、SiO2+4HF═SiF4↑+2H2O,说明了SiO2具有碱性 |
下列图象分别表示有关反应的反应过程与能量变化的关系 据此判断下列说法正确的是( )
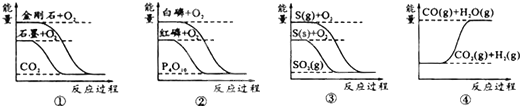

| A、石墨转变为金刚石是吸热反应 |
| B、白磷比红磷稳定 |
| C、CO (g)+H2O (g)=CO2 (g)+H2 (g)△H<0 |
| D、S (g)+O2 (g)=SO2 (g)△H1; S (s)+O2 (g)=SO2 (g)△H2,则△H1>△H2 |
0.5mol H2含有( )
| A、0.5 mol 个氢气分子 |
| B、6.02×1023个氢气分子 |
| C、3.01×1023个氢气分子 |
| D、3.01×1023个电子 |
 ③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中:
③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中:


