题目内容
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,已知某溶液中含有Fe3+、Cu2+和SO42-,设溶液中Cu2+的物质的量浓度为3.0mol?L-1,则Cu(OH)2开始沉淀时溶液的pH为 ,完全沉淀时溶液的pH为 ,通过计算确定pH=4时,Fe3+残存的浓度是: .(请写出计算过程lg3=0.48)
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:依据氢氧化铜饱和溶液中溶度积常数计算氢氧化铜开始沉淀溶液中的氢离子浓度计算,依据完全沉淀得到c(Cu2+)1×10-5 mol?L-1,计算c(OH-),然后计算c(H+),再计算pH即可,依据此pH=4,计算氢氧根的浓度,利用Fe(OH)3的溶度积Ksp=8.0×10-38计算残留铁离子的浓度.
解答:
解:Cu(OH)2的溶度积Ksp=3.0×10-20,溶液中CuSO4的浓度为3.0mol?L-1,c(Cu2+)=3.0mol?L-1;
依据溶度积常数c(Cu2+)×c2(OH-)=
=3.0×10-20 ;c2(OH-)=
=10-20;
得到c(OH-)=10-10mol/L,
依据水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=10-4mol/L,溶液pH=4,
则Cu(OH)2开始沉淀时溶液的pH为4;
残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,Cu(OH)2的溶度积Ksp=3.0×10-20,c(Cu2+)×c2(OH-)=3.0×10-20;c2(OH-)=
=3.0×10-15;
求得c(OH-)=5.47×10-8mol/L;
水溶液中的离子积c(H+)×c(OH-)=10-14,c(H+)=1.83×10-7mol/L,
则pH=6.7;
常温下Fe(OH)3的溶度积Ksp=8.0×10-38,c(Fe3+)×c3(OH-)=8.0×10-38,c(Fe3+)=
mol/L=8×10-8mol/L,
故答案为:4;6.7;8×10-8mol/L.
依据溶度积常数c(Cu2+)×c2(OH-)=
| 3×10-20 |
| 3.0 |
| 3×10-20 |
| 3.0 |
得到c(OH-)=10-10mol/L,
依据水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=10-4mol/L,溶液pH=4,
则Cu(OH)2开始沉淀时溶液的pH为4;
残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,Cu(OH)2的溶度积Ksp=3.0×10-20,c(Cu2+)×c2(OH-)=3.0×10-20;c2(OH-)=
| 3×10-20 |
| 1×10-5 |
求得c(OH-)=5.47×10-8mol/L;
水溶液中的离子积c(H+)×c(OH-)=10-14,c(H+)=1.83×10-7mol/L,
则pH=6.7;
常温下Fe(OH)3的溶度积Ksp=8.0×10-38,c(Fe3+)×c3(OH-)=8.0×10-38,c(Fe3+)=
| 8.0×10-38 |
| (1×10-10)3 |
故答案为:4;6.7;8×10-8mol/L.
点评:本题主要考查的是溶解沉淀的转化关系的分析应用以及pH的有关计算,题目难度中等.

练习册系列答案
相关题目
点燃的镁条伸入盛有下列气体的集气瓶中,能继续燃烧的是( )
①Cl2 ②O2 ③CO2 ④水蒸气.
①Cl2 ②O2 ③CO2 ④水蒸气.
| A、① | B、①② | C、①②③ | D、①②④ |
已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.30kJ?mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:下列说法正确的是( )
 | 0 | 1 | 2 | 3 |
| N2 | 1.50 | n1 | 1.20 | n3 |
| H2 | 4.50 | 4.20 | 3.60 | n4 |
| NH3 | 0 | 0.20 | n2 | 1.00 |
| A、反应进行到1小时时放出的热量为9.23kJ |
| B、反应3h内,反应速率v(N2)为0.17mol?L-1?h-1 |
| C、此温度下,该反应的平衡常数为0.037 |
| D、4h时,若再加入1molN2,达到新的平衡时,N2的转化率是原来的两倍 |
下列有机物的系统命名正确的是( )
A、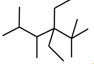 2,3,5,5-四甲基-4,4-二乙基己烷 |
B、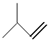 2-甲基-3-丁烯 |
C、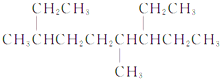 4,7-二甲基-3-乙基壬烷 |
D、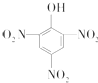 1,3,5-三硝基苯酚 |
如图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有 ( )
A、 |
B、 |
C、 |
D、 |
E、 |
某同学组装了如图所示的电化学装置,电极Ⅰ为Zn,其他电极均为Cu,则下列说法正确的是( )


| A、电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ |
| B、电极Ⅰ发生还原反应 |
| C、电极Ⅳ逐渐溶解 |
| D、电极Ⅲ的电极反应:Cu-2e-═Cu2+ |
 (1)可逆反应N2(g)+3H2(g)2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为
(1)可逆反应N2(g)+3H2(g)2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为