题目内容
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4L二氯甲烷含有NA个二氯甲烷分子 |
| B、1L 0.1mol/L乙酸溶液中H+数为0.1NA |
| C、17.6g丙烷中所含的极性共价键为3.2NA个 |
| D、1mol Na2O2 固体中含离子总数为4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标准状况下,二氯甲烷不是气体,不能使用标况下的气体摩尔体积计算22.4L二氯甲烷的物质的量;
B、1L 0.1mol/L乙酸的物质的量为0.1mol,醋酸为弱电解质,溶液中电离的氢离子浓度小于0.1mol;
C、丙烷分子中存在8个碳氢共价键,17.6g丙烷的物质的量为0.4mol,含有3.2mol碳氢键;
D、过氧化钠中的阴离子为过氧根离子,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子.
B、1L 0.1mol/L乙酸的物质的量为0.1mol,醋酸为弱电解质,溶液中电离的氢离子浓度小于0.1mol;
C、丙烷分子中存在8个碳氢共价键,17.6g丙烷的物质的量为0.4mol,含有3.2mol碳氢键;
D、过氧化钠中的阴离子为过氧根离子,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子.
解答:
解:A、标况下,二氯甲烷不是气体,题中条件无法计算22.4L二氯甲烷的物质的量及分子数,故A错误;
B、该溶液中含有溶质乙酸0.1mol,由于乙酸在溶液中部分电离出氢离子,所以溶液中氢离子的物质的量小于0.1mol,溶液中H+数小于0.1NA,故B错误;
C、17.6g丙烷的物质的量为:
=0.4mol,0.4mol丙烷中含有极性共价键的物质的量为:8×0.4mol=3.2mol,所含的极性共价键为3.2NA个,故C正确;
D、1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子,含离子总数为3NA,故D错误;
故选C.
B、该溶液中含有溶质乙酸0.1mol,由于乙酸在溶液中部分电离出氢离子,所以溶液中氢离子的物质的量小于0.1mol,溶液中H+数小于0.1NA,故B错误;
C、17.6g丙烷的物质的量为:
| 17.6g |
| 176g/mol |
D、1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子,含离子总数为3NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,阿伏加德罗常数是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容,注意明确标况下气体摩尔体积的使用条件、过氧化钠中的阴离子为过氧根离子.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
下列有关叙述正确的是( )
A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH
| ||
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) | ||
C、室温下向10 mL pH=3的醋酸溶液中加水稀释,溶液中
| ||
| D、在0.1 mol?L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)?2Z(g),各组分在不同时刻的浓度如下表:下列说法正确的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 2min末浓度/mol?L-1 | 0.08 | a | b |
| 平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、平衡时,X的转化率为20% |
| B、t℃时,该反应的平衡常数为40 |
| C、增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动 |
| D、前2min内,用Y的变化量表示的平均反应速率v(Y)=0.03mol?L-1?min-1 |
对下列各组物质关系的描述中正确的是( )
A、 与 与 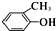 属于同素异形体 属于同素异形体 |
| B、CH3COOH与硬脂酸(C17H35COOH)属于同系物 |
C、 与 与  属于同一种物质 属于同一种物质 |
D、 与 与 属于同分异构体 属于同分异构体 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、能使甲基橙变黄的溶液中:Na+、K+、SO42-、Al3+ |
| B、pH=2的溶液中:Na+、ClO-、NH4+、SO42- |
| C、某透明澄清的溶液中:NH4+、Cu2+、NO3-、Cl- |
| D、0.1 mol?L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl- |
化学与人类生产、生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、光化学烟雾是氮氧化物受紫外线照射后产生的O3直接与空气中的一些碳氢化合物作用后生成的一种有毒烟雾 |
| B、石油液化气、汽油和石蜡的主要成分都是碳氢化合物 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
能在水溶液中大量共存的离子组是( )
| A、H+、Fe3+、SO42-、I- |
| B、H+、NH4+、HCO3-、NO3- |
| C、Ag+、K+、Cl-、SO42- |
| D、K+、AlO2-、Cl-、OH- |

