题目内容
4. 某同学设计了如图的实验:
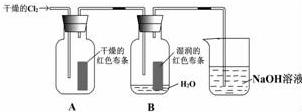
某同学设计了如图的实验:(1)氯气是一种黄绿色、有刺激性气味的有毒气体.若贮有氯气的钢瓶损坏,造成氯气泄露,在场人员除了采取有效措施外,其他人员应B(选字母).
A、向低洼处转移 B、向地势高处转移
(2)装置中通入Cl2后,集气瓶 A中干燥的红色布条无变化,集气瓶B中湿润的红色布条褪色;.由此可得出的结论是干燥Cl2没有漂白性,Cl2与水反应生成 HClO有漂白性.
(3)上述装置烧杯中盛放溶液的作用是吸收尾气,防止污染空气.写出烧杯中发生反应的化学方程式Cl2+2NaOH═NaCl+NaClO+H2O.
(4)Fe在Cl2中燃烧,生成棕褐色的烟,要检验其溶液中是否存在Fe3+,可向其中滴入几滴KSCN溶液,观察到的现象是溶液变为红色.若先向溶液中加入少量铁粉,充分反应后再滴入几滴KSCN溶液,结果观察不到此现象,原因是(用离子方程式表示)2Fe3++Fe=3Fe2+.
分析 (1)依据氯气是黄绿色气体,密度大于空气密度,有毒的物理性质解答;
(2)氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性,据此解答;
(3)氯气有毒,直接排放到空气中容易造成空气污染,氯气能够与氢氧化钠溶液反应,被氢氧化钠溶液吸收,二者反应生成氯化钠、次氯酸钠和水;
(4)三价铁离子遇到KSCN溶液显血红色,三价铁离子与铁反应生成二价铁离子.
解答 解:(1)氯气是黄绿色气体,密度大于空气密度,氯气泄露,向地势高处转移,故答案为:黄绿;B;
(2)氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性,所以装置中通入Cl2后,集气瓶 A中干燥的红色布条无变化,集气瓶B中湿润的红色布条褪色;
故答案为:褪色; 干燥Cl2没有漂白性,Cl2与水反应生成 HClO有漂白性;
(3)氯气有毒,直接排放到空气中容易造成空气污染,氯气能够与氢氧化钠溶液反应,被氢氧化钠溶液吸收,二者反应生成氯化钠、次氯酸钠和水,反应方程式:Cl2+2NaOH═NaCl+NaClO+H2O;
故答案为:吸收尾气,防止污染空气; Cl2+2NaOH═NaCl+NaClO+H2O;
(4)三价铁离子遇到KSCN溶液显血红色,通常用KSCN溶液检验三价铁离子,三价铁离子与铁反应生成二价铁离子,离子方程式:2Fe3++Fe=3Fe2+;
故答案为:溶液变为红色; 2Fe3++Fe=3Fe2+.
点评 本题考查了元素化合物知识,明确氯气、氯水的成分及性质是解题关键,注意三价铁离子、二价铁离子的影响,题目难度不大.

练习册系列答案
相关题目
19.某小组设计如图装置(部分夹持装置已略去),以探究潮湿的Cl2与Na2CO3反应得到固体物质的成分.
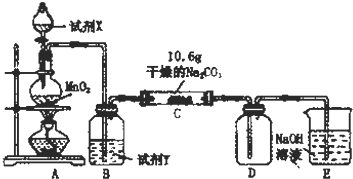
(1)A中制取Cl2的离子方程式4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中只含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究.
①提出合理假设.
假设1:存在两种成分:NaHCO3和NaCl;
假设2:存在三种成分:NaHCO3和NaCl、Na2CO3.
②设计方案,进行实验.写出实验步骤以及预期现象和结论.
限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
(3)已知C中有0.1mol Cl2参加反应.若假设一成立,可推知C中反应的化学方程式为2Cl2+H2O+2Na2CO3═2NaHCO3+2NaCl+Cl2O.

(1)A中制取Cl2的离子方程式4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中只含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究.
①提出合理假设.
假设1:存在两种成分:NaHCO3和NaCl;
假设2:存在三种成分:NaHCO3和NaCl、Na2CO3.
②设计方案,进行实验.写出实验步骤以及预期现象和结论.
限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水 至固体溶解,然后将所得溶液分别置于A、B试管中. | |
| 步骤2:向A试管中滴加适量BaCl2溶液. | a.若无明显现象,证明固体中不含Na2CO3 b.若溶液变浑浊,证明固体中含Na2CO3 |
| 步骤3:向B试管中滴加过量的稀硝酸,再滴加AgNO3溶液 | 若溶液变浑浊,证明固体中含有NaCl |



 .
. .
. .
. .
.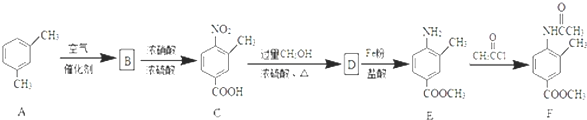
 ;由D→E的反应类型是还原反应.
;由D→E的反应类型是还原反应. .
. .
.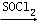 RCOCl.请写出以CH3CH2OH、
RCOCl.请写出以CH3CH2OH、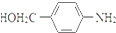 为原料,制备化合物
为原料,制备化合物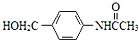 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C═CH2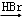 CH3CH2Br
CH3CH2Br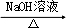 CH3CH2OH.
CH3CH2OH.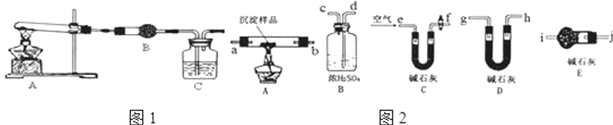
 .
. ,它是由极性共价键形成的极性分子.
,它是由极性共价键形成的极性分子. ,写出该反应的化学方程式IBr+H2O=HBr+HIO.
,写出该反应的化学方程式IBr+H2O=HBr+HIO.