题目内容
下列与化学反应能量变化相关的叙述正确的是( )
| A、放热反应的反应速率总是大于吸热反应的反应速率 |
| B、已知一定条件下石墨转化为金刚石吸收热量,则石墨比金刚石稳定 |
| C、对于吸热反应,生成物总能量一定低于反应物总能量 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
考点:吸热反应和放热反应,反应热和焓变
专题:化学反应中的能量变化
分析:A.反应速率是单位时间内物质浓度的变化,与反应的吸热、放热无关;
B.能量越低越稳定;
C.根据生成物总能量和反应物总能量的相对大小,把化学反应分为吸热反应和放热反应,吸热反应的生成物总能量高于反应物总能量,放热反应的生成物总能量低于反应物总能量;
D.△H与反应的条件无关.
B.能量越低越稳定;
C.根据生成物总能量和反应物总能量的相对大小,把化学反应分为吸热反应和放热反应,吸热反应的生成物总能量高于反应物总能量,放热反应的生成物总能量低于反应物总能量;
D.△H与反应的条件无关.
解答:
解:A.反应速率与反应的吸热、放热无关,所以放热反应的反应速率不一定大于吸热反应的反应速率,故A错误;
B.能量越低越稳定,石墨转化为金刚石吸收热量,石墨能量低,稳定,故B正确;
C.吸热反应的生成物总能量高于反应物总能量,放热反应的生成物总能量低于反应物总能量,故C错误;
D.同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同,故D错误.
故选B.
B.能量越低越稳定,石墨转化为金刚石吸收热量,石墨能量低,稳定,故B正确;
C.吸热反应的生成物总能量高于反应物总能量,放热反应的生成物总能量低于反应物总能量,故C错误;
D.同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同,故D错误.
故选B.
点评:本题主要考查了化学反应中能量变化,注意知识的积累,难度不大,注意能量低的物质更稳定即可解答.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列有关化学用语表示正确的是( )
A、NH4Br的电子式: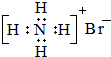 | ||
B、S原子的结构示意图: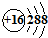 | ||
| C、乙醇的结构简式:C2H6O | ||
D、原子核内有18个中子的氯原子:
|
已知VmLAl2(SO4)3溶液中含有Al3+ag取出
mL溶液稀释到4VmL,则稀释后溶液中SO42-的物质的量浓度为( )
| V |
| 2 |
A、
| ||
B、
| ||
C、
| ||
| D、125a/54Vmol/L |
下列条件下,两瓶气体所含原子数一定相等的是( )
| A、同压强、同温度的O2和O3 |
| B、同温度、同体积的NH3和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |
若NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A、常温常压下,28g以任意比组成的CO与N2混合气体中含有2NA个原子 |
| B、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| C、常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA |
| D、标准状况下,11.2L H2O与8.5gNH3所含分子数相等 |
需加入氧化剂才能实现的是( )
| A、Fe3+→Fe2+ |
| B、Cl-→Cl2 |
| C、CuO→Cu |
| D、H2SO4→BaSO4 |
下列反应的离子方程式中,正确的是( )
| A、氢氧化钡溶液和稀硫酸Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、氯化铁溶液中加铁粉2Fe3++Fe=3Fe2+ |
| C、过量CO2通入NaOH溶液中CO2+2OH-=CO32-+H2O |
| D、少量CO2通入NaOH溶液中CO2+OH-=HCO3-+H2O |
下列变化中需加入氧化剂才能发生的是( )
| A、2Cl-→Cl2 |
| B、Fe3+→Fe2+ |
| C、Cu2+→Cu |
| D、KMnO4→MnO2 |