题目内容
下列有关化学用语表示正确的是( )
A、NH4Br的电子式: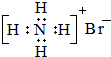 | ||
B、S原子的结构示意图: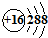 | ||
| C、乙醇的结构简式:C2H6O | ||
D、原子核内有18个中子的氯原子:
|
考点:电子式、化学式或化学符号及名称的综合,分子、原子、离子,原子结构示意图
专题:
分析:A.溴化铵中铵根离子和溴离子之间存在离子键,所以溴化铵是离子化合物,氮原子和氢原子之间存在共价键;
B.硫原子核外有16个电子,3个电子层,最外层电子数是6;
C.乙醇的结构简式要体现其官能团;
D.元素符号左上角数字表示质量数,左下角数字表示质子数.
B.硫原子核外有16个电子,3个电子层,最外层电子数是6;
C.乙醇的结构简式要体现其官能团;
D.元素符号左上角数字表示质量数,左下角数字表示质子数.
解答:
解:A.溴化铵是离子化合物,其电子式为: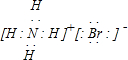 ,故A错误;
,故A错误;
B.硫原子核外有16个电子,3个电子层,最外层电子数是6,其原子结构示意图为: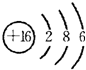 ,故B错误;
,故B错误;
C.乙醇分子是由乙基和羟基构成,其结构简式为CH3CH2OH,其分子式为C2H6O,故C错误;
D.元素符号左上角数字表示质量数,左下角数字表示质子数,原子核内有18个中子的氯原子其质量数是35,则该原子为1735Cl,故D正确;
故选D.
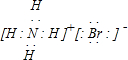 ,故A错误;
,故A错误;B.硫原子核外有16个电子,3个电子层,最外层电子数是6,其原子结构示意图为:
 ,故B错误;
,故B错误;C.乙醇分子是由乙基和羟基构成,其结构简式为CH3CH2OH,其分子式为C2H6O,故C错误;
D.元素符号左上角数字表示质量数,左下角数字表示质子数,原子核内有18个中子的氯原子其质量数是35,则该原子为1735Cl,故D正确;
故选D.
点评:本题考查了化学用语,涉及结构简式、原子结构示意图、电子式等知识点,有机物结构简式要体现其官能团,注意共价化合物和离子化合物电子式的区别,难度中等.

练习册系列答案
相关题目
下列两种无色试剂,不用其它试剂无法鉴别的是( )
| A、NaHCO3、HCl |
| B、Na2CO3、HCl |
| C、NaAlO2、H2SO4 |
| D、AlCl3、NaOH |
常温下,pH=11的氨水和pH=1的盐酸等体积混合后(不考虑溶液体积微小变化),恰好完全反应,则下列说法不正确的是( )
| A、反应后所得溶液呈酸性 |
| B、混合前两溶液的物质的量浓度相等 |
| C、原氨水中约有1%的含氮粒子为NH4+ |
| D、所得溶液中NH4+、NH3?H2O与NH3三种粒子的浓度之和为0.1 mol?L-1 |
某温度下,满足下列条件的溶液肯定呈酸性的是( )
| A、加酚酞显无色的溶液 |
| B、含有H+的溶液 |
| C、pH<7的溶液 |
| D、CH3COOH和NH3?H2O混合液,当c(CH3COO-)>c(NH4+)时 |
许多氧化物在一定条件下能与Na2O2反应,反应产物很有规律,如:Na2O2+SO2=Na2SO4;Na2O2+2SO3=2Na2SO4+O2.下列化学反应方程式肯定不正确的( )
| A、2Na2O2+2Mn2O7=4NaMnO4+O2↑ |
| B、2Na2O2+2N2O3=4NaNO2+O2 |
| C、2Na2O2+2N2O5=4NaNO3+O2↑ |
| D、Na2O2+2NO2=2NaNO3+O2 |
已知反应A2(g)+2B2(g)?2AB2(g)△H<0,下列说法正确的是( )
| A、升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| B、升高温度,正向反应速率增加,逆向反应速率减小 |
| C、达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D、达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
能证明SO2具有漂白性的是( )
| A、滴入酚酞的NaOH溶液中通入SO2气体红色消失 |
| B、溴水中通入SO2气体后溶液褪色 |
| C、酸性KMnO4溶液中通入SO2气体后溶液褪色 |
| D、品红溶液中通入SO2气体红色消失 |
常温下,下列各组微粒在指定溶液中一定能大量共存的是( )
A、
| ||
| B、0.1 mol/L AgNO3溶液:H+、K+、SO42-、I- | ||
| C、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- | ||
| D、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
下列与化学反应能量变化相关的叙述正确的是( )
| A、放热反应的反应速率总是大于吸热反应的反应速率 |
| B、已知一定条件下石墨转化为金刚石吸收热量,则石墨比金刚石稳定 |
| C、对于吸热反应,生成物总能量一定低于反应物总能量 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |