题目内容
以下可逆反应中,达到平衡后,通过升高温度可提高反应物转化率的是 ;通过增大压强可提高反应物转化率的是 ;改变压强,转化率不变的是 。
①A(s)+B(g) 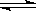 C(g), ΔH
< 0;
C(g), ΔH
< 0;
②N2(g)+3H2(g) 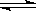 2NH3(g), ΔH < 0;
2NH3(g), ΔH < 0;
③2NO2(g) 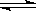 2NO(g) +O2(g),ΔH > 0;
2NO(g) +O2(g),ΔH > 0;
④2SO2(g)+O2(g) 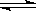 2SO3(g) ,ΔH
< 0。
2SO3(g) ,ΔH
< 0。
⑤CO(g)+NO2(g) 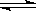 CO2(g) +NO(g),ΔH < 0;
CO2(g) +NO(g),ΔH < 0;
【答案】
③,②④,①⑤
【解析】
试题分析:通过升高温度可提高反应物转化率,说明该反应的正方应是吸热反应,所以答案选③;通过增大压强可提高反应物转化率,说明正方应是体积减小的,则答案选②④;改变压强,转化率不变,说明反应前后体积不变,答案选①⑤。
考点:考查外界条件对平衡状态的影响
点评:该题是高考中的常见题型,属于基础性试题的考查,试题灵活性强,难易适中。该题的关键是熟练掌握勒夏特列原理,并且能够灵活运用。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
现有可逆反应:2A(g)+2B(g)?C(g)+3D(g),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
| A、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同 | B、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的平均相对分子质量相同 | C、达到平衡时,Ⅰ途径A的平衡浓度等于Ⅱ途径A的平衡浓度 | D、达到平衡时,Ⅰ途径所得混合气密度为Ⅱ途径所得混合气密度的2倍 |
 2SO3在不同条件下进行时SO2的转化率:
2SO3在不同条件下进行时SO2的转化率: