题目内容
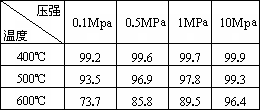
以下是反应2SO2+O2 2SO3在不同条件下进行时SO2的转化率:
2SO3在不同条件下进行时SO2的转化率:
从上表中你得到的启示?
(1)关于可逆反应的限度:
(2)提高该化学反应限度的途径有:
(3)要实现SO2的转化率为93.5%需控制的反应条件是
 2SO3在不同条件下进行时SO2的转化率:
2SO3在不同条件下进行时SO2的转化率:| 温度\压强 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600℃ | 73.7 | 85.8 | 89.5 | 96.4 |
(1)关于可逆反应的限度:
可逆反应中的反应物不能全部转化成生成物;(或可逆反应中的逆反应速率与正反应速率相等时,生成物和反应物的浓度不再改变,该反应就达到了一定的限度;或改变反应条件可以改变化学反应限度等)
可逆反应中的反应物不能全部转化成生成物;(或可逆反应中的逆反应速率与正反应速率相等时,生成物和反应物的浓度不再改变,该反应就达到了一定的限度;或改变反应条件可以改变化学反应限度等)
.(2)提高该化学反应限度的途径有:
增大压强或在一定范围内降低温度
增大压强或在一定范围内降低温度
.(3)要实现SO2的转化率为93.5%需控制的反应条件是
温度为500℃,压强为0.1MPa
温度为500℃,压强为0.1MPa
.分析:该反应为可逆反应,反应物不可能完全转化,由表中数据可知,压强和温度对平衡移动都有影响,增大压强SO2的转化率增大,但增大的幅度较小,升高温度SO2的转化率减小,说明该反应为放热反应,升高温度平衡向逆反应方向移动.
解答:解:(1)该反应为可逆反应,反应物不可能完全转化,无论压强和温度怎样变化,SO2的转化率都不可能为100%,当正逆反应速率相等时,生成物和反应物的浓度不再改变,该反应就达到了一定的限度,但改变外界条件下,平衡发生移动,
故答案为:可逆反应中的反应物不能全部转化成生成物;(或可逆反应中的逆反应速率与正反应速率相等时,生成物和反应物的浓度不再改变,该反应就达到了一定的限度;或改变反应条件可以改变化学反应限度等);
(2)由表中数据可知,压强和温度对平衡移动都有影响,增大压强SO2的转化率增大,但增大的幅度较小,升高温度SO2的转化率减小,说明该反应为放热反应,升高温度平衡向逆反应方向移动,所以提高该化学反应限度的途径有增大压强或在一定范围内降低温度,
故答案为:增大压强或在一定范围内降低温度;
(3)虽然反应放热,升高温度不利于平衡向正反应方向移动,但考虑催化剂的活性和反应速率不能太低,一般选择的温度为500℃,在0.1MPa时,SO2的转化率已经很大,若增大压强,对设备会有更高的要求,工业生成中常在0.1MPa下进行反应,故答案为:温度为500℃,压强为0.1MPa.
故答案为:可逆反应中的反应物不能全部转化成生成物;(或可逆反应中的逆反应速率与正反应速率相等时,生成物和反应物的浓度不再改变,该反应就达到了一定的限度;或改变反应条件可以改变化学反应限度等);
(2)由表中数据可知,压强和温度对平衡移动都有影响,增大压强SO2的转化率增大,但增大的幅度较小,升高温度SO2的转化率减小,说明该反应为放热反应,升高温度平衡向逆反应方向移动,所以提高该化学反应限度的途径有增大压强或在一定范围内降低温度,
故答案为:增大压强或在一定范围内降低温度;
(3)虽然反应放热,升高温度不利于平衡向正反应方向移动,但考虑催化剂的活性和反应速率不能太低,一般选择的温度为500℃,在0.1MPa时,SO2的转化率已经很大,若增大压强,对设备会有更高的要求,工业生成中常在0.1MPa下进行反应,故答案为:温度为500℃,压强为0.1MPa.
点评:本题考查化学平衡的影响因素,题目难度不大,注意分析表中数据,注重基础知识的积累.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
以下是反应2SO2+O2 2SO3在不同条件下进行时SO2的转化率:
2SO3在不同条件下进行时SO2的转化率:
从上表中你得到的启示?
(1)关于可逆反应的限度: .
(2)提高该化学反应限度的途径有: .
(3)要实现SO2的转化率为93.5%需控制的反应条件是 .
| 温度\压强 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600℃ | 73.7 | 85.8 | 89.5 | 96.4 |
(1)关于可逆反应的限度: .
(2)提高该化学反应限度的途径有: .
(3)要实现SO2的转化率为93.5%需控制的反应条件是 .
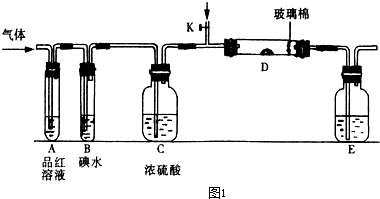
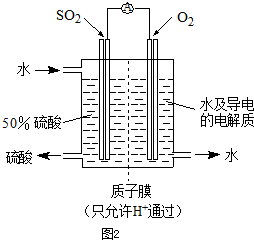
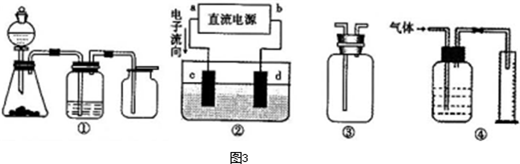
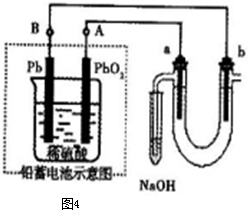
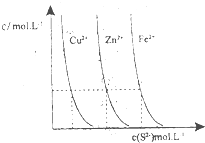 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题: