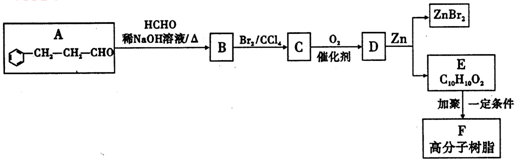
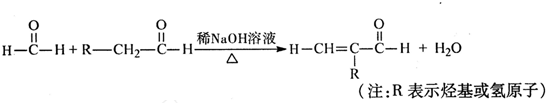
题目内容
下列实验装置图符合实验要求的是( )
A、 用NaOH溶液除去苯中少量的Br2 |
B、 实验室用乙醇和浓硫酸制备乙烯 |
C、 除去乙醇中少量的乙酸 |
D、 实验室制备并收集乙酸乙酯 |
考点:化学实验方案的评价,乙烯的实验室制法,物质的分离、提纯和除杂,乙酸乙酯的制取
专题:实验评价题
分析:A.溴单质能与氢氧化钠反应;
B.乙醇和浓硫酸制备乙烯反应在170℃下进行;
C.乙醇和乙酸互溶;
D.乙酸乙酯能与氢氧化钠反应.
B.乙醇和浓硫酸制备乙烯反应在170℃下进行;
C.乙醇和乙酸互溶;
D.乙酸乙酯能与氢氧化钠反应.
解答:
解:A.溴单质能与氢氧化钠反应,而苯不能,然后分液即可,故A正确;
B.乙醇和浓硫酸制备乙烯反应在170℃下进行,温度计应插入液面下,故B错误;
C.乙醇和乙酸互溶,不能用分液分离,故C错误;
D.乙酸乙酯能与氢氧化钠反应应用碳酸钠吸收,且导管不能插入液面下,故D错误.
故选A.
B.乙醇和浓硫酸制备乙烯反应在170℃下进行,温度计应插入液面下,故B错误;
C.乙醇和乙酸互溶,不能用分液分离,故C错误;
D.乙酸乙酯能与氢氧化钠反应应用碳酸钠吸收,且导管不能插入液面下,故D错误.
故选A.
点评:本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
已知反应:2SO2(g)+O2(g)
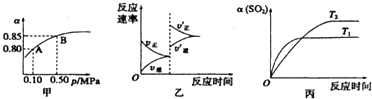
2SO3(g)△H<0某温度下,将2molSO2 和1molO2置于密闭容器中,反应到达平衡后,SO2的平衡转化率(a)与体系总压强(ρ)的关系如图甲所示,则下列说法正确的是( )
| 催化剂 |
| △ |

| A、由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B、点SO2、O2、SO3的平衡浓度之比为2:1:2 |
| C、达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D、压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
Mg、Cu和Al三种金属粉末的混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量NaOH溶液,再过滤,滤液中存在的离子有( )
| A、AlO2- |
| B、Al3+ |
| C、Mg2+ |
| D、Cu2+ |
下列推断正确的是( )
| A、金属单质与盐溶液的反应都是置换反应 |
| B、SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C、Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同 |
| D、C、N、S三种单质直接与O2反应都能生成两种以上氧化物 |
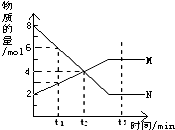 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2N?M |
| B、Bt2时,正逆反应速率相等,达到平衡 |
| C、t1时,N的浓度是M的浓度的2倍 |
| D、t3时,正反应速率大于逆反应速率 |
常温下,下列电解质溶液的有关叙述正确的是( )
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| C、pH═11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| D、同浓度同体积的强酸与强碱溶液混合后,溶液的pH=7 |
提供人体所需热能的最主要物质是( )
| A、蛋白质 | B、淀粉 | C、油脂 | D、水 |