题目内容
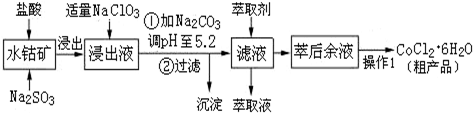
以明矾石[主要成分为K2SO4?Al2(SO4)3?2A12O3?6H2O]为原料生产硫酸铝晶体[Al2(SO4)3?18H2O]和明矾[KAl(SO4)2?12H2O]的实验流程如图所示:

两种不同形态的氧化铝的部分性质如表:
Al2(SO4)3、明矾在不同温度下的溶解度如表:
(1)“焙烧”温度过高,会导致硫酸铝晶体产量降低,其原因是 .
(2)从“母液”制备硫酸铝晶体的实验步骤为:① ;② ;③过滤、洗涤、干燥.
(3)测定硫酸铝晶体样品中Al2(SO4)3?18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25mL水中.
步骤2:加入c1mol?L-1 EDTA溶液V1mL(过量),煮沸、冷却,稀释至100mL.
步骤3:取25.00mL上述稀释液,滴加指示剂,用c2mol?L-1 Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗V2mL Pb(NO3)2标准溶液.
①步骤2中“稀释至100mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、 .
②根据上述数据计算,该样品中Al2(SO4)3?18H2O的质量分数为 .(用含字母的代数式表示).
(4)铝的阳极氧化法是把铝作为阳极,置于硫酸等电解液中,施加阳极电压进行电解,在铝的表面形成一层致密的氧化膜.
①电解过程中阳极的电极反应为 .
②取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是 .(用离子方程式表示)

两种不同形态的氧化铝的部分性质如表:
| 物质 | α-Al2O3 | γ-Al2O3 |
| 性质 | 不溶于水和酸 | 不溶于水,溶于强酸或强碱,加热至1200℃可转化为α-Al2O3 |
| 温度/℃ 溶解度/g | 0 | 20 | 40 | 60 | 80 | 100 |
| Al2(SO4)3 | 31.2 | 36.4 | 46.1 | 59.2 | 73.0 | 89.0 |
| 明矾 | 3.0 | 5.9 | 11.7 | 25 | 71 | 154 |
(2)从“母液”制备硫酸铝晶体的实验步骤为:①
(3)测定硫酸铝晶体样品中Al2(SO4)3?18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25mL水中.
步骤2:加入c1mol?L-1 EDTA溶液V1mL(过量),煮沸、冷却,稀释至100mL.
步骤3:取25.00mL上述稀释液,滴加指示剂,用c2mol?L-1 Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗V2mL Pb(NO3)2标准溶液.
①步骤2中“稀释至100mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
②根据上述数据计算,该样品中Al2(SO4)3?18H2O的质量分数为
(4)铝的阳极氧化法是把铝作为阳极,置于硫酸等电解液中,施加阳极电压进行电解,在铝的表面形成一层致密的氧化膜.
①电解过程中阳极的电极反应为
②取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
考点:制备实验方案的设计,电解原理,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:(1)温度过高导致γ-A12O3转化为难溶于硫酸的α-Al2O3;
(2)根据从溶液中制取晶体的步骤来分析;
(3)①根据仪器的作用选取仪器;
②根据硝酸铅的物质的量计算参加反应的EDTA的物质的量,再根据剩余EDTA的物质的量计算参加反应的铝离子的物质的量,根据质量分数公式计算其质量分数;
(4)①铝的阳极氧化法是把铝作为阳极,Al失电子生成氧化铝;
②铝离子与HCO3-发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳.
(2)根据从溶液中制取晶体的步骤来分析;
(3)①根据仪器的作用选取仪器;
②根据硝酸铅的物质的量计算参加反应的EDTA的物质的量,再根据剩余EDTA的物质的量计算参加反应的铝离子的物质的量,根据质量分数公式计算其质量分数;
(4)①铝的阳极氧化法是把铝作为阳极,Al失电子生成氧化铝;
②铝离子与HCO3-发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳.
解答:
解:(1)加热至1200℃γ-A12O3可转化为α-Al2O3,γ-A12O3不溶于水和酸,则“焙烧”温度过高,γ-A12O3转化为难溶于硫酸的α-Al2O3,会导致硫酸铝晶体产量降低,
故答案为:γ-A12O3转化为难溶于硫酸的α-Al2O3;
(2)从溶液中制取硫酸铝晶体时要经过蒸发浓缩溶液、冷却结晶、过滤、洗涤、干燥,故答案为:蒸发浓缩;冷却结晶;
(3)①配制一定物质的量浓度的溶液时,用100mL容量瓶配制溶液,用胶头滴管定容,故答案为:100 mL容量瓶、胶头滴管;
②硝酸铅和EDTA反应时需要EDTA的物质的量=10-3C2V2mol,那么100mL溶液中EDTA的物质的量=4×10-3C2V2mol,则和铝离子反应的EDTA的物质的量=10-3C1V1mol-4×10-3C2V2mol,EDTA和铝离子以1:1反应,所以铝离子的物质的量=10-3C1V1mol-4×10-3C2V2mol,Al2(SO4)3?18H2O的物质的量=0.5×(10-3C1V1mol-4×10-3C2V2mol),Al2(SO4)3?18H2O的质量=0.5×(10-3C1V1mol-4×10-3C2V2mol)×666g/mol=333(10-3C1V1-4×10-3C2V2)g,
其质量分数=
×100%,
故答案为:
×100%;
(4)①铝的阳极氧化法是把铝作为阳极,Al失电子生成氧化铝,则阳极的电极反应式为:2Al+3H2O-6e-═Al2O3+6H+;
故答案为:2Al+3H2O-6e-═Al2O3+6H+;
②铝离子与HCO3-发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳,反应的离子方程式为Al3++3HCO3-═Al(OH)3↓+3CO2↑;
故答案为:Al3++3HCO3-═Al(OH)3↓+3CO2↑.
故答案为:γ-A12O3转化为难溶于硫酸的α-Al2O3;
(2)从溶液中制取硫酸铝晶体时要经过蒸发浓缩溶液、冷却结晶、过滤、洗涤、干燥,故答案为:蒸发浓缩;冷却结晶;
(3)①配制一定物质的量浓度的溶液时,用100mL容量瓶配制溶液,用胶头滴管定容,故答案为:100 mL容量瓶、胶头滴管;
②硝酸铅和EDTA反应时需要EDTA的物质的量=10-3C2V2mol,那么100mL溶液中EDTA的物质的量=4×10-3C2V2mol,则和铝离子反应的EDTA的物质的量=10-3C1V1mol-4×10-3C2V2mol,EDTA和铝离子以1:1反应,所以铝离子的物质的量=10-3C1V1mol-4×10-3C2V2mol,Al2(SO4)3?18H2O的物质的量=0.5×(10-3C1V1mol-4×10-3C2V2mol),Al2(SO4)3?18H2O的质量=0.5×(10-3C1V1mol-4×10-3C2V2mol)×666g/mol=333(10-3C1V1-4×10-3C2V2)g,
其质量分数=
| 333(C1V1-4C2V2) |
| 1000m |
故答案为:
| 333(C1V1-4C2V2) |
| 1000m |
(4)①铝的阳极氧化法是把铝作为阳极,Al失电子生成氧化铝,则阳极的电极反应式为:2Al+3H2O-6e-═Al2O3+6H+;
故答案为:2Al+3H2O-6e-═Al2O3+6H+;
②铝离子与HCO3-发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳,反应的离子方程式为Al3++3HCO3-═Al(OH)3↓+3CO2↑;
故答案为:Al3++3HCO3-═Al(OH)3↓+3CO2↑.
点评:本题以铝的化合物为载体考查了物质间的反应、物质的分离和提纯、滴定原理的应用、电解原理的应用等知识点,明确物质之间的反应是解本题关键,再结合原子守恒来分析解答,题目综合性较强,注意利用基础知识细心分析解答,难度中等.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、金属钠和水的反应:Na+2H2O=Na++OH-+H2↑ |
| B、向次氯酸钙溶液中通入SO2:Ca2++2ClO-+H2O+SO2=CaSO3+2HClO |
| C、过量的铁与浓硝酸反应:Fe+6H++3NO3-=Fe3++3NO2↑+3H2O |
| D、过量的NaHSO4溶液与Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |

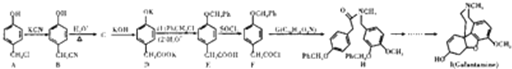

 发生类似反应①的反应,试写出其中一种产物的结构简式
发生类似反应①的反应,试写出其中一种产物的结构简式
 的同分异构体C的结构简式为
的同分异构体C的结构简式为 的合成路线图(无机试剂任选),合成路线流程图示例如下:CH3CH2OH
的合成路线图(无机试剂任选),合成路线流程图示例如下:CH3CH2OH