题目内容
欲用98%的浓硫酸(密度为1.84g?ml -3)配制成物质的量浓度为0.5mol?L-1的稀硫酸500ml.
(1)选用的主要仪器有:
①玻璃棒,②烧杯,③量筒,④胶头滴管,⑤ .
(2)请将下列各操作,按正确的序号填在横线上.
A.计算并用量筒量取浓H2SO4B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗涤玻璃棒烧杯2~3次也转移到容量瓶中
E.稀释浓H2SO4
F.将冷却到室温的溶液转移到容量瓶中
其操作正确的顺序依次为 .
(3)简要回答下列问题:
①所需浓硫酸的体积为 mL.
②如果实验室有15mL、20mL、50mL的量筒应选用 mL的量筒最好,忘记洗涤烧杯和玻璃棒,否则会使浓度 . (选填“偏高”、“偏低”、“无影响”,以下同.)
③定容时必须使溶液凹液面与刻度线相切,若俯视会使浓度 .
(1)选用的主要仪器有:
①玻璃棒,②烧杯,③量筒,④胶头滴管,⑤
(2)请将下列各操作,按正确的序号填在横线上.
A.计算并用量筒量取浓H2SO4B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗涤玻璃棒烧杯2~3次也转移到容量瓶中
E.稀释浓H2SO4
F.将冷却到室温的溶液转移到容量瓶中
其操作正确的顺序依次为
(3)简要回答下列问题:
①所需浓硫酸的体积为
②如果实验室有15mL、20mL、50mL的量筒应选用
③定容时必须使溶液凹液面与刻度线相切,若俯视会使浓度
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据用浓溶液配制一定物质的量浓度溶液步骤选用仪器;
(2)根据配制一定物质的量浓度的溶液步骤进行排序;
(3)质量百分数浓度转化为物质的量浓度,依据稀释前后溶质的物质的量不变计算需要的浓硫酸的体积;
依据需要浓硫酸体积选择合适的量筒;
分析不当操作对溶质的物质的量和溶液的体积,依据C=
进行误差分析.
(2)根据配制一定物质的量浓度的溶液步骤进行排序;
(3)质量百分数浓度转化为物质的量浓度,依据稀释前后溶质的物质的量不变计算需要的浓硫酸的体积;
依据需要浓硫酸体积选择合适的量筒;
分析不当操作对溶质的物质的量和溶液的体积,依据C=
| n |
| V |
解答:
解:(1)用浓溶液配制一定物质的量浓度溶液步骤:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,需要的仪器:烧杯、量筒、玻璃棒、500mL容量瓶、胶头滴管;
故答案为:500mL容量瓶;
(2)用浓溶液配制一定物质的量浓度溶液步骤:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀,所以正确的顺序为:AEFDCB;
故答案为:AEFDCB;
(3)①98%的浓硫酸(密度为1.84g?ml -3)的物质的量浓度C=
=18.4mol/L,设需要浓硫酸体积V,稀释前后溶质的物质的量不变,18.4mol/L×V=0.5mol?L-1×500mL,解得V=13.6mL;
故答案为:13.6;
②量取13.6mL浓硫酸,应选择20mL量筒;忘记洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液的浓度偏低;
故答案为:20;偏低;
③定容时必须使溶液凹液面与刻度线相切,若俯视会导致溶液的体积偏小,溶液的浓度偏高;
故答案为:偏高.
故答案为:500mL容量瓶;
(2)用浓溶液配制一定物质的量浓度溶液步骤:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀,所以正确的顺序为:AEFDCB;
故答案为:AEFDCB;
(3)①98%的浓硫酸(密度为1.84g?ml -3)的物质的量浓度C=
| 1000×1.84g?ml&;-3×98% |
| 98g/mol |
故答案为:13.6;
②量取13.6mL浓硫酸,应选择20mL量筒;忘记洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液的浓度偏低;
故答案为:20;偏低;
③定容时必须使溶液凹液面与刻度线相切,若俯视会导致溶液的体积偏小,溶液的浓度偏高;
故答案为:偏高.
点评:本题考查了配制一定物质的量浓度的溶液方法,题目难度不大,注意掌握配制一定物质的量浓度的溶液步骤是解题关键,注意误差分析的方法和技巧.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
化学工作者从有机反应RH+Cl2(g)
RCl(l)+HCl(g)受到启发提出的在农药和有机合成工业中可获得副产品HCl的设想已成为现实,试指出由上述反应产物分离得到盐酸的最佳方法是( )
| 光照 |
| A、水洗分液法 | B、蒸馏法 |
| C、升华法 | D、有机溶剂萃取法 |
铜与稀硝酸反应生成硝酸铜,一氧化氮和水,当生成1mol硝酸铜时,被还原的硝酸的物质的量为( )
A、
| ||
| B、1mol | ||
C、
| ||
D、
|
下列有关物质用途的说法中,不正确的是( )
| A、液氨可用做致冷剂,碱石灰可用于干燥氨气 |
| B、铁制器皿可用于盛放稀硫酸 |
| C、小苏打可用于治疗胃酸过多 |
| D、氯气可用于自来水消毒 |

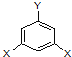 表示(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应的四种物质的结构简式
表示(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应的四种物质的结构简式