题目内容
7.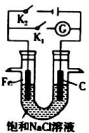 将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中形成如图装置:
将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中形成如图装置:①当开关K1闭合,则铁发生电化学腐蚀中的吸氧腐蚀.
②当开关K2闭合,则总反应的离子方程式为2C1-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+C12↑.
分析 ①当开关K1闭合,则构成原电池,在中性环境下,金属发生的是吸氧腐蚀;
②当开关K2闭合,则构成电解池,在阳极上发生失电子的氧化反应,在阴极上发生得电子的还原反应,根据电解原理来回答.
解答 解:①当开关K1闭合,则构成原电池,在中性环境下,金属发生的是吸氧腐蚀;故答案为:吸氧;
②当开关K2闭合,则构成电解池,铁是阴极,在阳极上氯离子发生失电子的氧化反应,在阴极上氢离子发生得电子的还原反应,总反应式:2C1-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+C12↑,故答案为:2C1-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+C12↑.
点评 本题考查了原电池和电解池的工作原理的应用,考查学生分析和解决问题的能力,综合性强,难度大.

练习册系列答案
相关题目
18.对溶液中的离子反应存在下列几种说法,其中正确的是( )
| A. | 不可能是氧化还原反应 | B. | 只能是复分解反应 | ||
| C. | 可能是置换反应 | D. | 可能是化合反应 |
15.下列各组烃的混合物,只要总质量一定,无论它们按何种比例混合,完全燃烧后生成的CO2和H2O都是恒量的是( )
| A. | C2H2、C2H4 | B. | C2H4、C3H6 | C. | C2H6、C3H8 | D. | CH4、C2H2 |
2.下列物质在给定条件下能实现转化的是( )
| A. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{H_{2}SO_{4}}{→}$Fe2(SO4)3 | |
| B. | 饱和食盐水$\stackrel{NH_{3}、CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | Cu2(OH)2CO3$\stackrel{H_{2}SO_{4}}{→}$CuSO4(aq)$\stackrel{Na}{→}$Cu |
12.下列有关物质的分类或归类正确的是( )
①混合物:水玻璃、水银
②化合物:氯化钙、烧碱、HD
③电解质:冰醋酸、硫酸钡
④同素异形体:H2O H2O2
⑤同位素:12C、13C、14C
⑥同分异构体: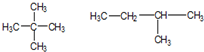
①混合物:水玻璃、水银
②化合物:氯化钙、烧碱、HD
③电解质:冰醋酸、硫酸钡
④同素异形体:H2O H2O2
⑤同位素:12C、13C、14C
⑥同分异构体:
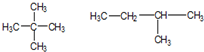
| A. | ①③④ | B. | ③⑤⑥ | C. | ①②③ | D. | ②⑥ |
19.某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( )
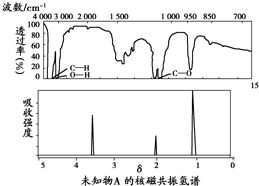

| A. | 由红外光谱可知,该有机物中至少有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子 | |
| C. | 若A的化学式为C2H6O,则其结构简式为CH3-O-CH3 | |
| D. | 由核磁共振氢谱无法得知其分子中的氢原子总数 |
17.在强酸性或强碱性溶液中都能大量共存的一组离子是( )
| A. | Ba2+、Fe3+、Br-、NO3- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、SO42-、Na+ | D. | Na+、K+、NO3-、SO42- |
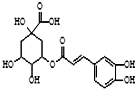 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.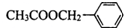 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: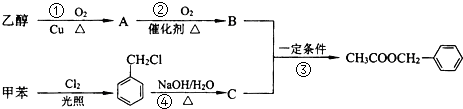
 +H2O$→_{△}^{氢氧化钠}$
+H2O$→_{△}^{氢氧化钠}$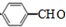 ;试写出遇FeCl3溶液显紫色,且符合以下条件的C的同分异构体的结构简式:
;试写出遇FeCl3溶液显紫色,且符合以下条件的C的同分异构体的结构简式: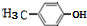
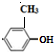 .
.