题目内容
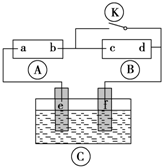 如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空:(1)电源A上的a为
(2)接通K点,使c、d两点短路,进行CuSO4溶液的电解,从通电开始算起经过一段时间后,两极均收集到22.4L气体(标准状况下),假定电解后溶液体积仍为500mL,此时溶液溶质为
考点:电解原理,原电池和电解池的工作原理
专题:电化学专题
分析:(1)接通电路后,B为电解池,c点显红色,说明C点有氢氧化钠生成,则c电极为阴极,d电极为阳极,连接阴极的原电池电极为负极;
(2)电解硫酸铜,根据两极反应结合两极均收集到22.4L气体(标准状况下),利用电子守恒计算溶液中溶质的物质的量浓度,电解质复原,出什么加什么,根据原子守恒确定加入的量.
(2)电解硫酸铜,根据两极反应结合两极均收集到22.4L气体(标准状况下),利用电子守恒计算溶液中溶质的物质的量浓度,电解质复原,出什么加什么,根据原子守恒确定加入的量.
解答:
解:(1)接通电路后,B为电解池,c点显红色,说明c点有氢氧化钠生成,则c电极为阴极,d电极为阳极,b为原电池负极,a为原电池正极,故答案为:正;
(2)电解硫酸铜,阳极上电极反应:4OH--4e-=2H2O+O2↑,生成1mol氧气消耗4mol氢氧根离子,阴极上电极方程式为:Cu2++2e-=Cu;2H++2e-═H2↑,在两极上产生气体都是22.4L,即1mol,所以转移电子是4mol,生成1mol氢气转移电子是2mol,减少氢离子1mol,所以溶液中氢离子的物质的量是3mol,生成的硫酸是1.5mol,铜离子全部放电,溶液中的溶质是硫酸,其物质的量浓度为
=3mol/L,为使电解质复原,应加入Cu(OH)2,根据铜元素守恒,加入的物质的量是1mol,
故答案为:H2SO4;3;Cu(OH)2;1.
(2)电解硫酸铜,阳极上电极反应:4OH--4e-=2H2O+O2↑,生成1mol氧气消耗4mol氢氧根离子,阴极上电极方程式为:Cu2++2e-=Cu;2H++2e-═H2↑,在两极上产生气体都是22.4L,即1mol,所以转移电子是4mol,生成1mol氢气转移电子是2mol,减少氢离子1mol,所以溶液中氢离子的物质的量是3mol,生成的硫酸是1.5mol,铜离子全部放电,溶液中的溶质是硫酸,其物质的量浓度为
| 1.5mol |
| 0.5L |
故答案为:H2SO4;3;Cu(OH)2;1.
点评:本题考查了电极原理的计算应用,为高频考点,侧重于学生的分析能力和计算能力的考查,注意电子守恒的计算应用和正确书写电极反应,明确电极的放电顺序为解答该题的关键,题目难度中等.

练习册系列答案
相关题目
下列关于物质的量、摩尔质量的叙述正确的是( )
| A、氢氧化钠的摩尔质量是40 g |
| B、1 mol H2O中含有2 mol氢和1 mol氧 |
| C、0.012 kg12C中含有约6.02×1023个碳原子 |
| D、2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
下列有关环境、健康及能源的叙述中,不正确的是( )
| A、氮的氧化物是光化学烟雾的主要污染物,二氧化碳是温室效应的主要污染物,所以他们的含量是空气质量报告的主要项目 |
| B、严格讲,“通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收 |
| C、开发利用新能源,合理利用工业生产的废热,是缓解能源危机的重要途径 |
| D、用二氧化硫、亚硝酸钠、苏丹红等化学药品“美化”后的食物“味美、色艳”,但添加剂超标,对人体危害极大 |
将含有0.400molCuSO4和0.200molKCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上析出19.2gCu,此时在另一电极上放出的气体在标准状况下的体积为( )
| A、5.60L |
| B、6.72L |
| C、4.48L |
| D、3.36L |
铜片放入稀硫酸中不溶解,加入下列物质后,能使溶液变蓝的是( )
| A、稀盐酸 | B、水 |
| C、硫酸钠 | D、硝酸钾 |
不用其它试剂,无法鉴别的一组溶液是( )
| A、NaOH和AlCl3 |
| B、Ca(HCO3)2和NaOH |
| C、NaAlO2和HNO3 |
| D、Na2CO3和HCl |
 工业上可采用电化学法利用H2S废气制取氢气,该法制氢过程的示意图如图所示,回答下列问题:
工业上可采用电化学法利用H2S废气制取氢气,该法制氢过程的示意图如图所示,回答下列问题: