题目内容
将含有0.400molCuSO4和0.200molKCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上析出19.2gCu,此时在另一电极上放出的气体在标准状况下的体积为( )
| A、5.60L |
| B、6.72L |
| C、4.48L |
| D、3.36L |
考点:电解原理
专题:电化学专题
分析:n(Cu)=
=0.3mol,阴极发生Cu2++2e-=Cu,可知阴极得到0.6mol电子,阳极发生:2Cl--2e-=Cl2↑、4OH--4e-=O2↑+2H2O,结合两极转移电子数目相等和电极方程式计算.
| 19.2g |
| 64g/mol |
解答:
解:n(Cu)=
=0.3mol,阴极发生Cu2++2e-=Cu,可知阴极得到0.6mol电子,阳极发生:2Cl--2e-=Cl2↑、4OH--4e-=O2↑+2H2O,
则生成n(Cl2)=0.1mol,转移电子0.2mol,则生成氧气转移电子0.4mol,生成氧气0.1mol,所以阳极共生成0.2mol气体,体积为4.48L,
故选C.
| 19.2g |
| 64g/mol |
则生成n(Cl2)=0.1mol,转移电子0.2mol,则生成氧气转移电子0.4mol,生成氧气0.1mol,所以阳极共生成0.2mol气体,体积为4.48L,
故选C.
点评:本题考查电解原理,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握电解方程式的书写,为解答该题的关键,难度中等.

练习册系列答案
相关题目
下列各组物质中,互称为同位素的是( )
| A、甲烷和乙烷 |
| B、氧气和臭氧 |
| C、126C和146C |
| D、正丁烷和异丁烷 |
下列有关化学用语正确的是( )
A、CO2的电子式 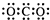 | ||
B、Cl-的结构示意图  | ||
| C、硫离子的核外电子排布式1s22s63s23p4 | ||
D、质量数为37的氯原子
|
某学生用0.1000mol?L-1标准NaOH溶液滴定未知浓度的盐酸,下列说法正确的是( )
| A、本实验可选石蕊作指示剂 |
| B、锥形瓶用水洗净后再用待测液润洗2~3次 |
| C、移液管取盐酸后,垂直放入稍倾斜的锥形瓶中并使管尖与内壁接触 |
| D、滴定过程中眼睛应始终注视滴定管内液面变化 |
下列各组物质,只用一种试剂即能区别开的是( )
| A、MgO、Al2O3、SiO2 |
| B、硫酸钾、碳酸钾、硫酸铝三种溶液 |
| C、氯化镁、氯化铝、氯化钠三种溶液 |
| D、硫酸铵、硝酸铵、氯化铵三种溶液 |
对于反应N2(g)+3H2(g)?2NH3(g),在一密闭容器中加入一定量的N2和H2,达到平衡时气体压强为P1,迅速缩小体积使气体压强为P2,一段时间后达到新的平衡,此时气体的压强为P3,则P1、P2、P3的大小关系( )
| A、P2>P1<P3 |
| B、P2>P3>P1 |
| C、P2>P1>P3 |
| D、P2>P1=P3 |
两种气态烃的混合气体10mL在50mL氧气里充分燃烧,生成液态水和体积为40mL的气体(气体体积均在同温同压下测定),则这两种烃不可能是( )
| A、C2H2和C2H6 |
| B、C2H2和C3H8 |
| C、CH4和C2H4 |
| D、C2H2和C2H4 |
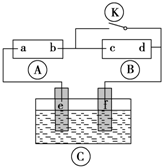 如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空: