题目内容
不用其它试剂,无法鉴别的一组溶液是( )
| A、NaOH和AlCl3 |
| B、Ca(HCO3)2和NaOH |
| C、NaAlO2和HNO3 |
| D、Na2CO3和HCl |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:如不用其它试剂就可鉴别,则可根据物质的颜色或对物质的进行相互滴加,滴加顺序不同,产生的现象不同,结合对应物质的性质解答该题.
解答:
解:A.将氯化铝溶液滴加到氢氧化钠溶液中,先无沉淀生成,当氯化铝滴加到一定程度时才有沉淀,但把氢氧化钠溶液滴加到氯化铝溶液中,立即产生沉淀,当氢氧化钠过量时沉淀溶解,滴加顺序不同,反应的现象不同,用其他试剂就可鉴别,故A不选;
B.Ca(HCO3)2和NaOH,无论滴加顺序如何,只反应生成碳酸钙沉淀,不能鉴别,故B选;
C.当硝酸少量时,离子反应方程式为H++AlO2-+H2O=Al(OH)3↓,当硝酸过量时,离子反应方程式为:4H++AlO2-=Al3++2H2O,所以反应现象不同,可鉴别,故C不选;
D.将盐酸滴加到碳酸钠溶液中,先无气体生成,当滴加盐酸一定量时开始生成气体,但把碳酸钠溶液滴加到盐硫酸中立即生成气体,滴加顺序不同,产生的现象不同,可不用其它试剂进行鉴别,故D不选.
故选B.
B.Ca(HCO3)2和NaOH,无论滴加顺序如何,只反应生成碳酸钙沉淀,不能鉴别,故B选;
C.当硝酸少量时,离子反应方程式为H++AlO2-+H2O=Al(OH)3↓,当硝酸过量时,离子反应方程式为:4H++AlO2-=Al3++2H2O,所以反应现象不同,可鉴别,故C不选;
D.将盐酸滴加到碳酸钠溶液中,先无气体生成,当滴加盐酸一定量时开始生成气体,但把碳酸钠溶液滴加到盐硫酸中立即生成气体,滴加顺序不同,产生的现象不同,可不用其它试剂进行鉴别,故D不选.
故选B.
点评:本题考查物质的检验、鉴别,题目难度中等,注意掌握常见物质的化学性质及检验、鉴别方法,把握物质的性质为解答该类题目的关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
对于反应N2(g)+3H2(g)?2NH3(g),在一密闭容器中加入一定量的N2和H2,达到平衡时气体压强为P1,迅速缩小体积使气体压强为P2,一段时间后达到新的平衡,此时气体的压强为P3,则P1、P2、P3的大小关系( )
| A、P2>P1<P3 |
| B、P2>P3>P1 |
| C、P2>P1>P3 |
| D、P2>P1=P3 |
两种气态烃的混合气体10mL在50mL氧气里充分燃烧,生成液态水和体积为40mL的气体(气体体积均在同温同压下测定),则这两种烃不可能是( )
| A、C2H2和C2H6 |
| B、C2H2和C3H8 |
| C、CH4和C2H4 |
| D、C2H2和C2H4 |
有氧化铁和氧化铜的混合物a g,加入2mol/L的硫酸溶液50mL时,恰好完全溶解.若将2ag这种混合物在氢气流中加热并充分反应,冷却后剩余固体的质量为( )
| A、0.8g |
| B、1.6ag |
| C、(2a-3.2)g |
| D、(2a-1.6)g |
常温下,下列有关电解质溶液的叙述正确的是( )
| A、等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7 |
| B、pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性 |
| C、pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg2=0.3) |
| D、将10mLpH=a的盐酸与100mLpH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13 |
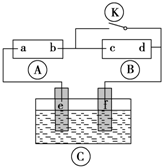 如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空: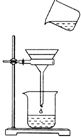 已知粗盐中含有泥沙,硫酸钠、氯化钙杂质,在进行提纯的过程中,某学生设计了如图所示的实验操作.回答下列问题:
已知粗盐中含有泥沙,硫酸钠、氯化钙杂质,在进行提纯的过程中,某学生设计了如图所示的实验操作.回答下列问题: