题目内容
15.五种短周期元素的某些信息如表所示:| 元素 | 有关信息 |
| X | 最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
| Y | M层上有3个电子 |
| Z | 短周期元素中原子半径最大的主族元素 |
| W | 其单质是淡黄色固体 |
| Q | 最高正价与最低负价代数和为6 |
| A. | 简单离子的半径大小顺序为:W>Q>Z>Y | |
| B. | W单质在氧气中燃烧后的产物不能使品红溶液褪色 | |
| C. | X、W和氢三种元素形成的化合物中只有共价键 | |
| D. | Z与W元素只能形成原子个数比为2:1的化合物 |
分析 短周期元素中,X最高价氧化物对应的水化物能与其气态氢化物反应生成盐,则X为N元素;Y元素原子M层上有3个电子,则Y为Al;Z是短周期元素中原子半径最大的主族元素,则Z为Na;W单质是淡黄色固体,则W为S元素;Q最高正价与最低负价代数和为6,则Q为Cl,结合元素周期律与元素化合物性质解答.
解答 解:短周期元素中,X最高价氧化物对应的水化物能与其气态氢化物反应生成盐,则X为N元素;Y元素原子M层上有3个电子,则Y为Al;Z是短周期元素中原子半径最大的主族元素,则Z为Na;W单质是淡黄色固体,则W为S元素;Q最高正价与最低负价代数和为6,则Q为Cl,
A.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Cl->Na+>Al3+,故A正确;
B.硫在氧气中燃烧生成二氧化硫,二氧化硫具有漂白性,可以使品红溶液褪色,故B错误;
C.N、S、H三种元素形成(NH4)2S,属于离子化合物,含有离子键和共价键,故C错误;
D.Na与S元素可以形成Na2S,也可以形成Na2S2,前者原子个数比为2:1,后者原子个数之比为1:1,故D错误,
故选A.
点评 本题考查结构性质位置关系应用,明确元素推断是解题关键,注意对基础知识的全面掌握,侧重于考查学生的分析能力和对基础知识的应用能力,题目难度中等.

练习册系列答案
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
5.少量SO2通入“84消毒液”中,(84消毒液是一种以NaClO为主的高效消毒剂)其离子反应方程式最合理的是( )
| A. | H2SO3+ClO-→2 H++SO42-+Cl- | B. | SO2+ClO-+H2O→2 H++SO42-+Cl- | ||
| C. | SO2+ClO-+H2O→SO32-+HClO | D. | SO2+ClO-+2OH-→SO42-+Cl-+H2O |
6.有一无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、CO32-、MnO4-中的一种或几种.为确定其成分,进行如下实验:
①取部分溶液,逐滴滴入NaOH溶液至过量并微热,只观察到白色沉淀先增多后又部分溶解,无其它明显现象;
②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生.
下列推断正确的是( )
①取部分溶液,逐滴滴入NaOH溶液至过量并微热,只观察到白色沉淀先增多后又部分溶解,无其它明显现象;
②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生.
下列推断正确的是( )
| A. | 肯定有Al3+、Mg2+、Cl-,可能有K+ | |
| B. | 肯定有Al3+、Mg2+,可能有CO32- | |
| C. | 肯定有Al3+、Mg2+、Cl-,肯定没有NH4+ | |
| D. | 肯定有Al3+、Cl-,可能有Mg2+ |
7.鼠尾草酚用于防治骨质疏松,鼠尾草酸可两步转化得到鼠尾草酚,下列说法正确的是( )
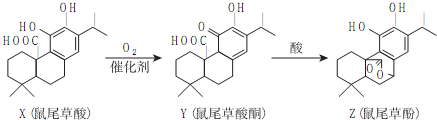

| A. | X、Z属于芳香族化合物 | |
| B. | X、Y、Z均能与FeCl3溶液发生显色反应 | |
| C. | 1molX或1molZ与NaOH溶液反应,均最多消耗3molNaOH | |
| D. | Z能与溴的四氯化碳溶液发生加成反应 |
5.下列实验不能达到预期目的是( )
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、Al Cl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | NaCO3溶液中加入稀H2SO4 | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与盐酸反应 | 比较铁、铜的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/L的硫酸溶液中,乙同学将电极放入6mol/L的NaOH溶液中,实验装置如图所示:
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/L的硫酸溶液中,乙同学将电极放入6mol/L的NaOH溶液中,实验装置如图所示: