题目内容
氯化钠、氯化镁、硫酸镁,三种盐配成的混合液1L,若钠离子为0.1mol,镁离子0.25mol,氯离子0.2mol,则硫酸根的物质的量为 .
考点:电解质在水溶液中的电离
专题:守恒法
分析:根据溶液中存在的电荷守恒结合溶液显示中性等知识来回答.
解答:
解:在体积为1L的中性溶液中,氢离子和氢氧根离子的量是相等的,其他离子存在的守恒:n(Na+)+2n(Mg2+)=n(Cl-)+2n(SO42-),即0.1mol+0.25mol×2=0.2mol+2n(SO42-),解得:n(SO42-)=0.2mol,
故答案为:0.2mol.
故答案为:0.2mol.
点评:本题考查学生关于溶液中电荷守恒的灵活应用知识,难度不大.

练习册系列答案
相关题目
下列实验操作中错误的是( )
| A、碘水中萃取碘时,往分液漏斗中先后加入碘水和酒精,充分振荡静置后分液 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液操作时,应先从分液漏斗的下口放出下层液体,再从上口倒出上层液体 |
| D、蒸发时,当蒸发皿中的水只残留少许时,停止加热,利用余热将剩余水分蒸干 |
在反应H2+CuO
Cu+H2O中,还原产物是( )
| ||
| A、H2 |
| B、CuO |
| C、Cu |
| D、H2O |
关于化学键的说法正确的是( )
| A、一切物质都存在化学键 |
| B、不同元素组成的多原子分子里的化学键一定是极性键 |
| C、离子键的实质是阴阳离子间的静电引力 |
| D、由非金属元素组成的化合物不一定只含共价键 |
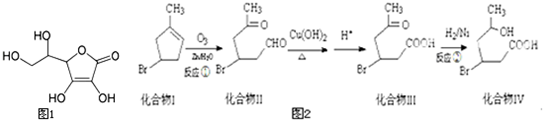
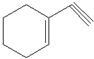 (1)某有机化合物分子结构式如图采取sp2杂化的C原子有
(1)某有机化合物分子结构式如图采取sp2杂化的C原子有 )发生类似反应①的反应,得到一种环状化合物Ⅵ(一种香料),化合物Ⅵ的结构简式为
)发生类似反应①的反应,得到一种环状化合物Ⅵ(一种香料),化合物Ⅵ的结构简式为