题目内容
下列关于甲烷与氯气发生取代反应所得生成物的说法正确的是( )
| A、都是有机物 |
| B、都不溶于水 |
| C、有一种气态物质,其余都是液体 |
| D、有一种是无机物其余都是有机物 |
考点:甲烷的化学性质
专题:有机化学基础
分析:甲烷与氯气在光照的条件下发生取代反应,生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,四种氯代烷中,除了一氯甲烷为气体,其余都为液体,据此解答.
解答:
解:A.生成的氯化氢为无机物,故A错误;
B.甲烷与氯气发生取代反应所得生成物氯化氢易溶于水,故B错误;
C.氯化氢、一氯甲烷都是气态,故C错误;
D.一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,只有氯化氢为无机物,故D正确;
故选:D.
B.甲烷与氯气发生取代反应所得生成物氯化氢易溶于水,故B错误;
C.氯化氢、一氯甲烷都是气态,故C错误;
D.一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,只有氯化氢为无机物,故D正确;
故选:D.
点评:本题考查了甲烷的性质,题目难度不大,明确甲烷发生取代反应的原理和产物是解题关键,注意氯代烷的物理性质.

练习册系列答案
相关题目
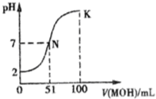 常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、HA为一元强酸 | ||
| B、N点水的电离程度小于K点水的电离程度 | ||
C、随着MOH溶液的滴加,比值
| ||
| D、若K点对应的溶液的PH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L |
①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+K2SO4+7H2O
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4
下列结论正确的是( )
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+K2SO4+7H2O
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4
下列结论正确的是( )
| A、①②③均是氧化还原反应 |
| B、氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2 |
| C、反应②中氧化剂与还原剂的物质的量之比为6:1 |
| D、反应③中0.1mol还原剂共失去电子数为6.02×1023 |
类比是化学学习中一种常见的思维方式,以下使用类比的方法得出的结论正确的是( )
| A、CO2可以与Ca(ClO)2反应生成CaCO3和HClO,类比出SO2也可以与Ca(ClO)2反应生成CaSO3和HClO |
| B、实验室使用浓硫酸与NaCl固体共热的方法制取HCl,类比出也可以采用浓硫酸与KNO3固体共热的方法制取HNO3 |
| C、由CaCO3溶解度小于Ca(OH)2,类比出MgCO3溶解度小于Mg(OH)2 |
| D、碱金属单质的熔沸点从上到下依次降低,类比出卤素单质的熔沸点也是从上到下依次降低 |
已知下列元素的原子半径
根据以上数据,磷原子的半径(10-10m)可能是( )
| 原子 | N | S | O | Si |
| 半径(10-10m) | 0.75 | 1.02 | 0.74 | 1.17 |
| A、0.80 | B、1.10 |
| C、1.20 | D、0.70 |
某核反应堆使用液体钠铝合金作载热介质,下列说法错误的是( )
| A、该合金的熔点低于金属钠的熔点 |
| B、若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Na)≥n(Al) |
| C、若将钠铝合金投入FeCl3溶液,有Fe(OH)3沉淀生成 |
| D、将m g不同组成的钠铝合金投入足量盐酸溶液中,若放出H2越多,则铝的质量分数越小 |
下列叙述不正确的是( )
| A、NaHSO4、Na2O2晶体中的阴、阳离子个数比均为1:2 |
| B、有离子键的化合物一定是离子化合物 |
| C、某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H8-2m+nR或RH8-2m+n |
| D、元素周期表中L层电子为奇数的元素所在族序数与该元素原子的L层电子数相等 |
 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如下图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如下图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )| A、A膜是阳离子交换膜 |
| B、通电后,海水中阴离子往b电极处运动 |
| C、通电后,b电极上产生无色气体,溶液中出现白色沉淀 |
| D、通电后,a电极的电极反应式为4OH--4e-═O2↑+2H2O |
下列叙述与分子间作用力无关的是( )
| A、气体物质加压或降温时能凝成固体 |
| B、干冰易升华 |
| C、氟、氯、溴、碘单质的熔、沸点依次升高 |
| D、氯化钠的熔点较高 |