题目内容
12. 如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )
如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )| A. | 紫色石蕊溶液变红色,说明SO2呈酸性 | |
| B. | 品红溶液褪色,说明SO2具有漂白性 | |
| C. | 溴水橙色褪去,体现了SO2的还原性 | |
| D. | 含酚酞的NaOH溶液红色变浅,表明SO2能够和NaOH反应 |
分析 A.SO2不能漂白酸碱指示剂;
B.SO2具有漂白性,能使品红溶液褪色;
C.SO2具有还原性,Br2具有强氧化性,二者发生氧化还原反应生成HBr和硫酸;
D.SO2属于酸性氧化物,SO2和NaOH溶液反应生成亚硫酸钠而降低溶液碱性.
解答 解:A.二氧化硫和水反应生成亚硫酸,亚硫酸电离出氢离子而使其溶液呈酸性,紫色石蕊试液遇酸变红色,所以溶液呈红色,二氧化硫不显酸性,故A错误;
B.SO2和有色物质反应生成无色物质而具有漂白性,所以品红溶液褪色体现二氧化硫的漂白性,故B正确;
C.SO2具有还原性,Br2具有强氧化性,二者发生氧化还原反应生成HBr和硫酸,反应方程式为Br2+SO2+2H20=2HBr+H2SO4,该反应体现二氧化硫的还原性,故C正确;
D.SO2属于酸性氧化物,SO2和NaOH溶液反应生成亚硫酸钠而降低溶液碱性,所以将二氧化硫通入含有酚酞的NaOH溶液中,NaOH溶液会褪色,该现象说明二氧化硫属于酸性氧化物能够和NaOH反应,故D正确;
故选A.
点评 本题考查二氧化硫的性质,知道二氧化硫、次氯酸漂白原理的区别,注意二氧化硫不能漂白酸碱指示剂,为易错点,题目难度中等.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
11.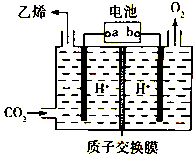 CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题.如图所示电解装置可将CO2转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极.下列有关说法正确的是( )
CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题.如图所示电解装置可将CO2转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极.下列有关说法正确的是( )
 CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题.如图所示电解装置可将CO2转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极.下列有关说法正确的是( )
CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题.如图所示电解装置可将CO2转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极.下列有关说法正确的是( )| A. | a为电池的正极 | |
| B. | 电解过程中H+移向阳极 | |
| C. | 反应前后溶液的pH保持不变 | |
| D. | 阴极反应式:2CO2+12H++12e-=C2H4+4H2O |
3.煤作为燃料有两种途径:
Ⅰ.C(s)+O2(g)═CO2(g)△H1<0
Ⅱ.C(s)+H2O(g)═CO(g)+H2(g)△H2>0
2CO(g)+O2(g)=2CO2(g△H3<0
2H2(g)+O2(g)═2H2O(g)△H4<0请回答:
(1)途径Ⅰ放出的热量=途径Ⅱ放出的热量(填“>”、“<”或“=”).
(2)△H1、△H2、△H3、△H4之间关系的数学表达式是△H1=△H2+$\frac{1}{2}$(△H3+△H4)
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表所示:
试回答下列问题:
①在一个温度恒定固定容积的密闭容器中发生上述反应,反应达到平衡的标志是cd
(填序号)
a.体系的压强不再改变 b.体系的密度不再改变 c.各气体的浓度不再改变
d.各气体的质量分数不再改变 e.反应速率v(CO):v(H2)=1:1
②上述反应的正反应是放热反应(填“放热”或“吸热”);
400℃时反应H2(g)+CO2(g)?CO(g)+H2O(g)的化学平衡常数数值是0.1;
③830℃时,在2L的密闭容器中加入4mol CO(g)和6mol H2O(g)发生反应,10分钟达到平衡,此10分钟内用H2表示的平均反应速率是0.12mol/(L•min);达到平衡时CO的转化率是60%.
(4)汽车尾气净化中的一个反应如:
NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.4kJ/mol
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是C

Ⅰ.C(s)+O2(g)═CO2(g)△H1<0
Ⅱ.C(s)+H2O(g)═CO(g)+H2(g)△H2>0
2CO(g)+O2(g)=2CO2(g△H3<0
2H2(g)+O2(g)═2H2O(g)△H4<0请回答:
(1)途径Ⅰ放出的热量=途径Ⅱ放出的热量(填“>”、“<”或“=”).
(2)△H1、△H2、△H3、△H4之间关系的数学表达式是△H1=△H2+$\frac{1}{2}$(△H3+△H4)
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表所示:
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①在一个温度恒定固定容积的密闭容器中发生上述反应,反应达到平衡的标志是cd
(填序号)
a.体系的压强不再改变 b.体系的密度不再改变 c.各气体的浓度不再改变
d.各气体的质量分数不再改变 e.反应速率v(CO):v(H2)=1:1
②上述反应的正反应是放热反应(填“放热”或“吸热”);
400℃时反应H2(g)+CO2(g)?CO(g)+H2O(g)的化学平衡常数数值是0.1;
③830℃时,在2L的密闭容器中加入4mol CO(g)和6mol H2O(g)发生反应,10分钟达到平衡,此10分钟内用H2表示的平均反应速率是0.12mol/(L•min);达到平衡时CO的转化率是60%.
(4)汽车尾气净化中的一个反应如:
NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.4kJ/mol
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是C

17.下列有关实验操作、现象、解释和结论都正确的是( )
| 选项 | 操 作 | 现 象 | 解释、结论 |
| A | 把过量的Fe粉中加入硝酸中充分反应,滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
| C | 定容时不小心加水超过容量瓶的刻度线,立即用滴管吸去多余的部分 | 液体凹液面与刻度线相平 | 配制溶液的浓度不受影响 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
1.下列有关化学用语的表示正确的是( )
| A. | NH4Cl的电子式: | B. | Cl-的结构示意图: | ||
| C. | 葡萄糖的实验式:CH2O | D. | 对硝基苯酚的结构简式: |

 可与甲醇充分反应,反应后有机产物的名称为:对苯二甲酸二甲酯
可与甲醇充分反应,反应后有机产物的名称为:对苯二甲酸二甲酯 .
. ,
, .
.