题目内容
300℃时,将2mol A和2mol B两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g)?2C(g)+2D(g);△H>0,2min末达到平衡,生成0.8mol D.
(1)在2min末时,B的平衡浓度为 ,D的平均反应速率为 .
(2)如果在相同的条件下,上述反应从逆反应方向进行,开始时若加入C、D各4/3mol.若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B mol.
(1)在2min末时,B的平衡浓度为
(2)如果在相同的条件下,上述反应从逆反应方向进行,开始时若加入C、D各4/3mol.若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)根据生成D的物质的量,计算参加反应的A、B的物质的量,进而计算平衡时B的物质的量,根据c=
计算B的平衡浓度,根据速率等于
计算D的平均反应速率;
(2)由方程式可知反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,据此判断应加入的物质及该物质的量物质的量.
| n |
| V |
| △C |
| △t |
(2)由方程式可知反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,据此判断应加入的物质及该物质的量物质的量.
解答:
解:(1)2min末反应达到平衡状态,生成0.8molD,则参加反应的A、B的物质的量都是0.8mol,平衡时B的物质的量=2mol-0.8mol=1.6mol,故B的平衡浓度=
=0.8mol/L,v(D)=
=0.2mol/(L?min),
故答案为:0.8mol/L;0.2 mol/(L?min);
(2)该反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,开始加入C和D各
mol,由化学方程式3A(g)+B(g)?2C(g)+2D(g)可知转化到左边,可以得到A为
mol×
=2mol,得到B为
mol×
=
mol,故还需要加入B的物质的量为2mol-
mol=
mol;
故答案为:
.
| 1.6mol |
| 2L |
| ||
| 2min |
故答案为:0.8mol/L;0.2 mol/(L?min);
(2)该反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,开始加入C和D各
| 4 |
| 3 |
| 4 |
| 2 |
| 3 |
| 2 |
| 4 |
| 3 |
| 1 |
| 2 |
| 2 |
| 3 |
| 2 |
| 3 |
| 4 |
| 3 |
故答案为:
| 4 |
| 3 |
点评:本题考查化学平衡的有关计算、影响化学平衡的因素、等效平衡等,难度中等,注意等效平衡规律的掌握.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
2007年我国首颗探月卫星“嫦娥一号”发射成功,其绕月飞行的目的之一是探测月球土壤中核聚变材料
He的含量.据报道,月球的土壤中吸附着数百万吨的
He,每百吨
He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以
He的形式存在.下列说法正确的是( )
3 2 |
3 2 |
3 2 |
4 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列叙述正确的是( )
A、
| ||||
| B、CO2和CO属于同素异形体,所以性质不同 | ||||
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | ||||
| D、C(石墨,s)=C(金刚石,s);△H>0.所以石墨比金刚石稳定 |
在氢气与氧气燃烧的过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氧气中的化学键消耗的能量为Q2kJ,形成1mol水中的化学键释放的能量为Q3kJ.下列关系式中,正确的是( )
| A、Q1+Q2<Q3 |
| B、Q1+Q2>2Q3 |
| C、2Q1+Q2>2Q3 |
| D、2Q1+Q2<2Q3 |
下列叙述正确的是(NA为阿伏伽德罗常数)( )
| A、标况下,22.4L苯的分子数为NA |
| B、10.0mL 18mol/L的浓硫酸中氢离子数为0.36NA |
| C、6.4gS6与S8的混合物中所含S原子数一定为0.2NA |
| D、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |

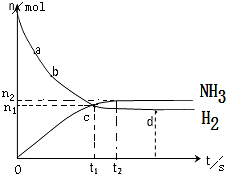 合成氨工业对国民经济和社会发展具有重要的意义.一定温度下,在2L的密闭容器中加入一定量的N2和H2,发生合成氨反应,其中n(NH3)和n(H2)随时间变化的关系如图所示.
合成氨工业对国民经济和社会发展具有重要的意义.一定温度下,在2L的密闭容器中加入一定量的N2和H2,发生合成氨反应,其中n(NH3)和n(H2)随时间变化的关系如图所示.