题目内容
17.下列氢化物中稳定性最强的是( )| A. | H2O | B. | NH3 | C. | H2S | D. | HF |
分析 元素的非金属性越强,对应的氢化物越稳定,以此来判断.
解答 解:非金属性:F>O>N>S,元素的非金属性越强,对应的氢化物越稳定,则热稳定性:HF>H2O>NH3>H2S,故氢化物稳定性最强的是HF,
故选D.
点评 本题考查元素周期律知识,题目难度不大.要注意元素的非金属性越强,对应的氢化物越稳定.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
8.下列液体温度均处在25℃,有关叙述正确的是( )
| A. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 将1 L 0.1 mol•L-1的Ba(OH)2溶液稀释为2 L,pH=12 | |
| D. | pH=8的NaOH溶液稀释100倍,其pH=6 |
5.向以下四种溶液中分别持续通入CO2,最终得到沉淀的一组是( )
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
| A. | ①③④ | B. | ②③④ | C. | ③④ | D. | ①②③ |
12.下列元素中,原子半径最大的是( )
| A. | 锂 | B. | 钠 | C. | 氟 | D. | 氯 |
2.下列叙述正确的是( )
| A. | C2H2分子内含有极性键,但C2H2分子是非极性分子 | |
| B. | 分子晶体、原子晶体一定含有共价键,离子晶体一定含有离子键 | |
| C. | 气态氢化物的稳定性随着其相对分子量的增大而增强 | |
| D. | 某非金属元素从游离态变成化合态时,该元素一定被还原 |
9.与CO32-不是等电子体的是( )
| A. | SO3 | B. | BF3 | C. | NO3- | D. | PCl3 |
6.X、Y、Z是原子序数依次增大的短周期主族元素,X2-、Z+都与Mg2+具有相同的核外电子层结构,下列说法中正确的是( )
| A. | Y元素位于第二周期第ⅦA族或0族 | |
| B. | X、Y、Z三种元素中非金属性最强的是X元素 | |
| C. | Y的最高氧化物对应的水化物是已知酸中最强的酸 | |
| D. | Z分别与X、Y形成的化合物都是离子化合物 |
7.下列关于有机物的命名中正确的是( )
| A. | 2-甲基-3-丁烯 | B. | 2-乙基戊烷 | ||
| C. | 3-甲基-1,3-丁二烯 | D. | 2,3-二甲基己烷 |
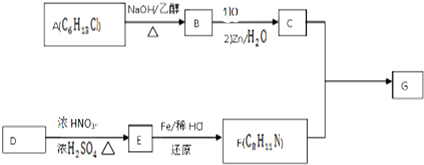
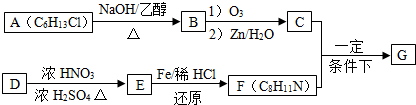
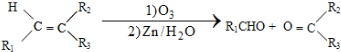
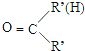 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$
 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$  +H2O.
+H2O. .
. .(写出其中的一种的结构简式).
.(写出其中的一种的结构简式). $\stackrel{反应条件1}{→}$H$\stackrel{反应条件2}{→}$I$→_{一定条件下}^{C}$J$\stackrel{还原}{→}$
$\stackrel{反应条件1}{→}$H$\stackrel{反应条件2}{→}$I$→_{一定条件下}^{C}$J$\stackrel{还原}{→}$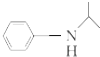
 .
.