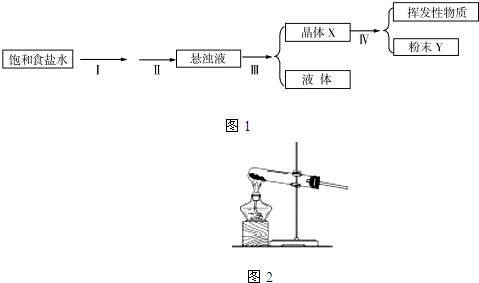
题目内容
配制一定物质的量浓度的溶液时,会导致所配溶液浓度偏大的操作是( )
| A、在用蒸馏水洗涤烧杯时,洗涤液未全部注入容量瓶中 |
| B、定容摇匀后,发现液面低于刻度线,又加水到刻度线 |
| C、定容时俯视刻度线 |
| D、用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 |
考点:溶液的配制
专题:化学实验基本操作
分析:A.洗液未全部注入容量瓶中,损失了部分溶质,浓度偏小;
B.摇匀时,液体会沾在瓶颈上,使液面低于刻度线,若再加入水,体积会变大,浓度偏小;
C.定容时俯视刻度线,溶液实际不到刻度线,体积偏小,浓度偏大;
D.不影响溶质的量,也不影响溶液的体积,浓度不变.
B.摇匀时,液体会沾在瓶颈上,使液面低于刻度线,若再加入水,体积会变大,浓度偏小;
C.定容时俯视刻度线,溶液实际不到刻度线,体积偏小,浓度偏大;
D.不影响溶质的量,也不影响溶液的体积,浓度不变.
解答:
解析:A项,洗液未全部注入容量瓶中,损失了部分溶质,浓度偏小;故A错误;
B项,摇匀时,液体会沾在瓶颈上,使液面低于刻度线,若再加入水,体积会变大,浓度偏小;故B错误;
C项,定容时俯视刻度线,溶液实际不到刻度线,体积偏小,浓度偏大;故C正确;
D项,不影响溶质的量,也不影响溶液的体积,浓度不变,故D错误;
故选C.
B项,摇匀时,液体会沾在瓶颈上,使液面低于刻度线,若再加入水,体积会变大,浓度偏小;故B错误;
C项,定容时俯视刻度线,溶液实际不到刻度线,体积偏小,浓度偏大;故C正确;
D项,不影响溶质的量,也不影响溶液的体积,浓度不变,故D错误;
故选C.
点评:本题考查了配制一定物质的量浓度的溶液的操作方法及误差分析,难度不大,要求学生掌握配制一定物质的量浓度的溶液的正确操作方法,能够根据错误操作对c=
的影响判断产生的误差.
| n |
| V |

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
25℃某浓度的盐酸、氯化铵溶液中水电离出的氢离子浓度分别为1.0×10-amol?L-1、1.0×10-bmol?L-1,则这两种溶液的pH之和为( )
| A、14-a+b |
| B、14+a+b |
| C、14-a-b |
| D、14+a-b |
下列比较中,正确的是( )
| A、等温等物质的量浓度溶液中,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大 |
| B、0.2 mol/L NH4Cl溶液和0.1 mol/LNaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C、物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、同浓度的下列溶液中:①NH4Al(SO4)2 ②NH4Cl ③CH3COONH4 ④NH3?H2O,c(NH4+)由大到小的顺序是①>②>③>④ |
下列叙述中正确的是( )
| A、可用托盘天平准确称取3.15gNaCl |
| B、实验室中可用燃烧法处理CO、H2、H2S等可燃性尾气 |
| C、测定中和热时,环形玻璃搅拌棒可用铜丝代替或直接用温度计搅拌 |
| D、Fe2+与Fe[(CN)6]3-反应生成Fe3[Fe(CN)6]2蓝色沉淀,该反应可用于Fe2+的检验 |
聚丙烯酸钠(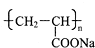 )具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )
)具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )
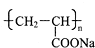 )具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )
)具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )| A、聚丙烯酸钠属于混合物 |
| B、聚丙烯酸钠属于天然有机高分子化合物 |
| C、聚丙烯酸钠可用于生产“尿不湿” |
| D、路面喷洒聚丙烯酸钠溶液能抑制扬尘,一定程度上能预防雾霾和PM2.5 |
在《化学1》P.44的【拓展视野】中介绍了二氧化氯是一种新型灭菌消毒剂.以下反应可制得ClO2:2NaClO3+Na2SO3+H2SO4?2ClO2+2Na2SO4+H2O.对于该反应,下列说法中正确的是( )
| A、该反应是复分解反应 |
| B、Na2SO3发生氧化反应 |
| C、H2SO4是氧化剂 |
| D、NaClO3是还原剂 |
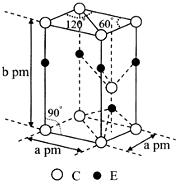 前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价层电子均已成对.
前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价层电子均已成对.