题目内容
下列关于锶(Sr,核电核数为38)的单质(密度为2.50g/cm3),一定错误的是( )
| A、颗粒状单质锶投入CuSO4溶液中,能置换出金属铜 |
| B、颗粒状的单质锶跟稀硫酸反应,不如钠和水反应那么剧烈 |
| C、锶在纯氧中点燃可燃烧 |
| D、锶的碳酸盐难溶于水 |
考点:金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:根据锶和金属镁、钙是一个主族,同主族元素的单质性质具有相似性并结合同主族元素性质的递变规律来回答.
解答:
解:A、锶和金属镁、钙是一个主族,活泼性强于钙,金属钙和盐溶液反应时先是和水之间反应,所以锶投入CuSO4溶液中,会先是和水反应,不会置换出金属铜,故A错误;
B、金属锶的活泼性比金属钠弱,所以颗粒状的单质锶跟稀硫酸反应,不如钠和水反应那么剧烈,故B正确;
C、根据金属没可以和氧气之间的反应可以知道锶在纯氧中点燃可燃烧,故C正确;
D、碳酸镁、碳酸钙是白色难溶于水的沉淀,所以碳酸锶是难溶于水的,故D正确.
故选A.
B、金属锶的活泼性比金属钠弱,所以颗粒状的单质锶跟稀硫酸反应,不如钠和水反应那么剧烈,故B正确;
C、根据金属没可以和氧气之间的反应可以知道锶在纯氧中点燃可燃烧,故C正确;
D、碳酸镁、碳酸钙是白色难溶于水的沉淀,所以碳酸锶是难溶于水的,故D正确.
故选A.
点评:本题考查学生金属元素性质的递变规律知识,注意同主族元素性质的相似性和递变性是关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图:
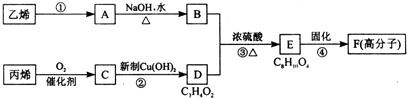
关于该过程的相关叙述正确的是( )

关于该过程的相关叙述正确的是( )
| A、反应④的反应类型是缩聚反应 |
| B、物质A是卤代烃 |
| C、物质B催化氧化后可以得到乙醛 |
| D、1 mol物质D最多可以消耗2 mol NaOH |
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A、1mol?L -1的NaClO溶液中含有ClO-的数目为NA |
| B、常温常压下,分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| C、标准状况下,11.2 L CH3CH2OH 中含有的氢原子数目为3NA |
| D、室温下,1L pH=13的Ba(OH)2溶液中,OH-离子数目为0.2NA |
有关说法正确的是( )
| A、0.1mol/L NH4C1溶液加蒸馏水稀释,溶液的pH不断减小 |
| B、常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
| C、NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO42-) |
| D、0.1mol/L的NaHA溶液,其pH=4时:c(HA-)>c(H+)>c(H2A)>c(A2-) |
物质在反应中可表现氧化性、还原性、酸性、碱性等,下面反应的划线物质中,能在同一反应中同时表现上述两种或两种以上性质的有( )
①3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
③8NH3+3Cl2═6NH4Cl+N2
④NaH+H2O═NaOH+H2↑
⑤2Na2O2+2H2O═4NaOH+O2↑
①3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
③8NH3+3Cl2═6NH4Cl+N2
④NaH+H2O═NaOH+H2↑
⑤2Na2O2+2H2O═4NaOH+O2↑
| A、仅有①② | B、仅有①③④⑤ |
| C、仅有①③⑤ | D、全部 |
下列说法不正确的是( )
| A、单质Si能与NaOH溶液反应 |
| B、向氯化铝溶液中滴加过量氢氧化钠可制得Al(OH)3 |
| C、在反应:4CuS+5O2═2Cu2O+4SO2中,CuS既是氧化剂又是还原剂 |
| D、向AgCl的饱和液中加少量KI溶液可以比较AgCl和AgI的溶解度大小 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、0.5 molAl与足量盐酸反应转移电子数为1NA |
| B、标准状况下,11.2L SO3所含的分子数为0.5NA |
| C、0.1molCH4所含的电子数为1NA |
| D、46gNO2和N2O4的混合物含有的分子数为1NA |