题目内容
18.下列叙述正确的是( )| A. | NaCl溶液在电流作用下电离成Na+与Cl- | |
| B. | 溶于水后能电离出H+的化合物都是酸 | |
| C. | 氯化氢溶于水能导电,但液态氯化氢不能导电 | |
| D. | NaCl固体不导电是由于不含Na+、Cl- |
分析 A.氯化钠为电解质,在水溶液中可发生电离;
B.酸式盐可电离出氢离子;
C.氯化氢为共价化合物,熔融状态下不导电;
D.氯化钠为离子化合物,固体不导电.
解答 解:A.氯化钠为电解质,在水溶液中可发生电离,无需在电流下,故A错误;
B.酸式盐可电离出氢离子,如硫酸氢钠,故B错误;
C.氯化氢为共价化合物,水溶液可导电,但熔融状态下不导电,故C正确;
D.氯化钠为离子化合物,固体不导电,熔融状态下可电离出自由移动的离子,故D错误.
故选C.
点评 本题考查电解质的电离以及导电性,为高频考点,侧重考查学生的分析能力,注意把握离子化合物和共价化合物的区别,把握电解质的电离特点,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.化学与生活密切相关,下列说法错误的是( )
| A. | 将燃油车改为燃气车有利于减少污染物排放 | |
| B. | 含氟牙膏能有效预防龋齿,且其中所加氟化物的量宜多不宜少 | |
| C. | 糖类、油脂及蛋白质都含有C、H、O元素 | |
| D. | 酸雨浸蚀的土壤中加入熟石灰,可对该土壤进行修复 |
6.检查氯化氢气体中是否混有氯气?可采用的方法是( )
| A. | 用干燥的有色布条检验 | B. | 将气体通入硝酸银溶液 | ||
| C. | 用干燥的蓝色石蕊试纸检验 | D. | 用湿润的碘化钾淀粉试纸检验 |
7.下列叙述正确的是( )
| A. | NaHCO3溶液中:c(H+)+c(Na+)═c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)一样多 | |
| C. | 0.2mol•L-1 HCl溶液与等体积0.05 mol•L-1 Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 向10 mL 0.10mol•L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
16.化学在自然资源的开发和利用中具有重要的意义,下列对其认识不正确的是( )
| A. | 利用化学知识和化学规律,人们可以更好的开发和利用资源 | |
| B. | 人们在开发和利用资源的过程中,对环境造成了污染,化学对此无能为力 | |
| C. | 利用化学知识和化学规律,人们可以制取更多物质,丰富物质世界 | |
| D. | 人们对资源的开发和利用过程中,时刻不能忘记资源的可持续性发展 |

 ,名称是环己烷.
,名称是环己烷.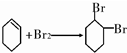 .
.



 ;溴化钠中存在的化学键是离子键,
;溴化钠中存在的化学键是离子键, ,溴化钠的电离方程式为NaBr=Na++Br-.检验某固体试样中是否有Br-的方法为取固体试样少许用蒸馏水溶解,再滴加硝酸酸化的硝酸银溶液,若有浅黄色沉淀生成,则证实有Br-存在.
,溴化钠的电离方程式为NaBr=Na++Br-.检验某固体试样中是否有Br-的方法为取固体试样少许用蒸馏水溶解,再滴加硝酸酸化的硝酸银溶液,若有浅黄色沉淀生成,则证实有Br-存在.

 ,则①是E,②是D,③是A(填字母),其中装置E的作用是i观察气体的通入速率ⅱ混合氯气和氮气ⅲ除去氯气中的氯化氢
,则①是E,②是D,③是A(填字母),其中装置E的作用是i观察气体的通入速率ⅱ混合氯气和氮气ⅲ除去氯气中的氯化氢