题目内容
9.根据下面的反应路线及所给信息填空.
A的结构简式是
 ,名称是环己烷.
,名称是环己烷.①的反应类型是取代反应.④的反应类型是消去反应.反应③的化学方程式是
 .
.
分析 ①为为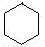 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,发生取代反应生成一氯环己烷,故A为
+HCl,发生取代反应生成一氯环己烷,故A为 ,②为卤代烃的消去反应,③为双键的加成反应生成B为
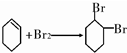
,②为卤代烃的消去反应,③为双键的加成反应生成B为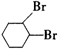 ,④为
,④为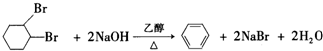 ,属于消去反应,以此来解答.
,属于消去反应,以此来解答.
解答 解:A的结构简式是 ,名称是环己烷;①的反应类型是取代反应,④的反应类型是消去反应,反应③的化学方程式为
,名称是环己烷;①的反应类型是取代反应,④的反应类型是消去反应,反应③的化学方程式为 ,
,
故答案为: ;环己烷;取代反应;消去反应;
;环己烷;取代反应;消去反应; .
.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团的变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
5.甲、乙两瓶氨水的浓度分别为1mol•L-1、0.1mol•L-1,则两瓶氨水中c(OH)-之比( )
| A. | 等于10 | B. | 小于10 | C. | 大于10 | D. | 等于1 |
17.下列有关物质性质的说法错误的是( )
| A. | 热稳定性:HCl>HI | B. | 原子半径:Na>Mg | ||
| C. | 酸性:H2SO4>HClO4 | D. | 还原性:S2->Cl- |
4. 如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应.钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应.钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
 如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应.钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应.钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A. | 甲、乙、丙都属于氧化还原反应 | |
| B. | 甲反应的离子方程式为Na+2H2O═Na++2OH-+H2↑ | |
| C. | 甲、乙、丙充分反应后所得溶液的质量分数分别为w1、w2、w3,则2w1=w2=w3 | |
| D. | 丙充分反应,能产生0.05 mol O2,转移电子0.1 mol |
14.下列实验方案,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 氯气的氧化性 | 将湿润的淀粉KI试纸放于充满Cl2的集气瓶口,试纸变蓝 |
| B | 配制480mL 0.2mol/L NaOH溶液 | 准确称量NaOH固体4.0g溶于水,配制成500mL溶液 |
| C | 比较H2CO3和H2SO4的酸性强弱 | 室温下,用pH试纸测定浓度为 0.1mol/L Na2CO3溶液和 0.1mol/L Na2SO4溶液的pH |
| D | 鉴别Na2CO3溶液与NaHCO3溶液 | 分别加入Ca(OH)2溶液看是否产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
1.下列说法不正确的是( )
| A. | 氢键存在于分子之间,也存在于分子之内 | |
| B. | 对于组成和结构相似的分子,其范德华力随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 冰熔化时只破坏分子间作用力 |
18.下列叙述正确的是( )
| A. | NaCl溶液在电流作用下电离成Na+与Cl- | |
| B. | 溶于水后能电离出H+的化合物都是酸 | |
| C. | 氯化氢溶于水能导电,但液态氯化氢不能导电 | |
| D. | NaCl固体不导电是由于不含Na+、Cl- |
7. 如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )
如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )
 如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )
如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )| A. | X代表的元素处于第ⅥA族 | |
| B. | Y的最低负化合价是-3 | |
| C. | M元素的最高价氧化物对应的水化物的化学式是HMO3 | |
| D. | 气态氢化物的稳定性:N>Z |
 .
. +nCO2$\stackrel{催化剂}{→}$
+nCO2$\stackrel{催化剂}{→}$
